题目内容
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol SiO2晶体中有2NA个Si-O键 |
| B、0.5 mol I-被氧化时失去的电子数为0.5NA |
| C、在0℃,压强为1.01×105 Pa时,11.2 L SO3所含原子数目为2NA |
| D、常温常压下,48 g O3含有氧原子数为3NA |
考点:阿伏加德罗常数
专题:
分析:A、1mol二氧化硅含有4molSi一O键;
B、依据碘离子可以被氧化为碘单质或碘酸根来分析;
C、标况下,SO3为液态;
D、根据臭氧的质量计算出物质的量,再计算出氧原子的物质的量;
B、依据碘离子可以被氧化为碘单质或碘酸根来分析;
C、标况下,SO3为液态;
D、根据臭氧的质量计算出物质的量,再计算出氧原子的物质的量;
解答:
解:A、在SiO2晶体中,1个Si原子结合4个O原子,故1molSiO2晶体含有4molSi一O键,故A错误;
B、碘离子可以被氧化为碘单质或碘酸根,所以氧化产物不定,故B错误;
C、标况下,SO3为液态,故C错误;
D、48gO3的物质的量是1.5mol,含有3mol氧原子,含有氧原子数为3NA,故D正确;
故选D.
B、碘离子可以被氧化为碘单质或碘酸根,所以氧化产物不定,故B错误;
C、标况下,SO3为液态,故C错误;
D、48gO3的物质的量是1.5mol,含有3mol氧原子,含有氧原子数为3NA,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述正确的是( )
| A、合金材料中不可能含有非金属元素 |
| B、SiO2为酸性氧化物,故不能与任何酸发生化学反应 |
| C、用砂纸打磨过的铝箔放在洒精灯焰上不燃烧,说明铝不易与O2反应 |
| D、FeCl2、FeCl3、Fe(OH)3三种物质都可以直接通过化合反应制取 |
下列说法不正确的是( )
| A、塑料袋在全球“失宠”,有偿使用成为风尚,是因为塑料袋填埋占用土地,且难以降解 |
| B、酶催化反应具有高效、专一、条件温和等特点,化学模拟生物酶对绿色化学、环境保护及节能减排具有重要意义 |
| C、2012年诺贝尔化学奖授予两位美国科学家罗伯特?莱夫科维茨和布莱恩?克比尔卡,以表彰他们在“G蛋白偶联受体研究”中取得的重大成就 |
| D、道尔顿、李比希、汤姆生、卢瑟福、玻尔等科学家的研究不断更新人们对原子结构的认识 |
下列变化中,属于放热反应的是( )
| A、H2O(g)═H2O(l)△H=-44kJ/mol |
| B、2HI(g)═H2(g)+I2(g)△H=+14.9kJ/mol |
C、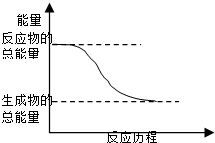 能量变化如图所示的化学反应 |
| D、形成化学键时放出能量的化学反应 |
设NA为阿伏加德罗常数,下列叙述正确的是( )
| A、1mol铁与足量盐酸完全反应转移的电子数目为3NA |
| B、28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为NA |
| C、100mL 1mol/L FeCl3溶液中含有Fe3+为0.1NA |
| D、32g氧气和32g臭氧(O3)所含有的氧原子数之比为2:3 |
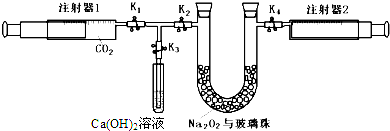
 (1)某矿石由几种常见氧化物组成,组成这些氧化物的元素在地壳中的含量都很丰富.向该矿石混合粉末中加入过量的氢氧化钠溶液,过滤得可用作红色涂料的红棕色固体和无色溶液,然后向所得溶液中滴入盐酸,所得沉淀的质量与所加盐酸的体积的关系如图所示:
(1)某矿石由几种常见氧化物组成,组成这些氧化物的元素在地壳中的含量都很丰富.向该矿石混合粉末中加入过量的氢氧化钠溶液,过滤得可用作红色涂料的红棕色固体和无色溶液,然后向所得溶液中滴入盐酸,所得沉淀的质量与所加盐酸的体积的关系如图所示: