题目内容
下列叙述正确的是( )
| A、合金材料中不可能含有非金属元素 |
| B、SiO2为酸性氧化物,故不能与任何酸发生化学反应 |
| C、用砂纸打磨过的铝箔放在洒精灯焰上不燃烧,说明铝不易与O2反应 |
| D、FeCl2、FeCl3、Fe(OH)3三种物质都可以直接通过化合反应制取 |
考点:合金的概念及其重要应用,硅和二氧化硅,铝的化学性质,铁的氧化物和氢氧化物
专题:元素及其化合物
分析:A.依据合金概念就是两种或两种以上的金属(或金属跟非金属)熔合而成的具有金属特性的物质;
B.SiO2为酸性氧化物,但能和氢氟酸反应;
C.铝与氧气反应生成氧化铝,其熔点较高;
D.化合反应指由两种或两种以上的物质生成一种新物质的反应,结合元素化合物的性质判断.
B.SiO2为酸性氧化物,但能和氢氟酸反应;
C.铝与氧气反应生成氧化铝,其熔点较高;
D.化合反应指由两种或两种以上的物质生成一种新物质的反应,结合元素化合物的性质判断.
解答:
解:A.合金材料中可能含有金属元素,非金属元素,如生铁,故A错误;
B.SiO2为酸性氧化物,SiO2和氢氟酸反应SiO2+4HF=SiF4+2H2O,故B错误;
C.铝与氧气反应生成氧化铝,其熔点较高,则观察不到燃烧,但铝易被氧化,故C错误;
D.铁与氯化铁反应生成氯化亚铁,铁与氯气化合生成氯化铁,氢氧化亚铁与氧气、水化合生成氢氧化铁,故D正确;
故选D.
B.SiO2为酸性氧化物,SiO2和氢氟酸反应SiO2+4HF=SiF4+2H2O,故B错误;
C.铝与氧气反应生成氧化铝,其熔点较高,则观察不到燃烧,但铝易被氧化,故C错误;
D.铁与氯化铁反应生成氯化亚铁,铁与氯气化合生成氯化铁,氢氧化亚铁与氧气、水化合生成氢氧化铁,故D正确;
故选D.
点评:本题考查了合金、酸性氧化物、氧化铝、氢氧化铁等物质的性质分析,积累化学知识,掌握铁、硅、铝等元素化合物的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
下列实验操作说法不正确的是( )
| A、实验室蒸馏石油时,冷凝管水流方向应从上到下与蒸汽流动方向相同 |
| B、蒸发结晶时不必将溶液加热到蒸干 |
| C、萃取操作必须在分液漏斗中进行 |
| D、用剩的药品应收集起来放回指定的回收处 |
已知X、Y、Z、W四种短周期主族元素在周期表中相对位置如图所示,下列说法不正确的是( )
| X | Y |
| Z | W |
| A、Y原子形成的简单离子半径一定比X原子形成的简单离子半径小 |
| B、W的原子序数可能是Y的原子序数的3倍 |
| C、W的气态氢化物的稳定性一定比Y的强 |
| D、若Z元素最高价氧化物的水化物是强酸,则W元素的单质具有强氧化性 |
25℃时,pH=2的酸和pH=12的碱溶液等体积混合后,恢复至原温,溶液呈酸性.其原因可能是( )
| A、生成了一种强酸弱碱盐 |
| B、等浓度的强酸和弱碱溶液反应 |
| C、浓的弱酸溶液和稀的强碱溶液反应 |
| D、浓的强酸和稀的强碱溶液反应 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol SiO2晶体中有2NA个Si-O键 |
| B、0.5 mol I-被氧化时失去的电子数为0.5NA |
| C、在0℃,压强为1.01×105 Pa时,11.2 L SO3所含原子数目为2NA |
| D、常温常压下,48 g O3含有氧原子数为3NA |
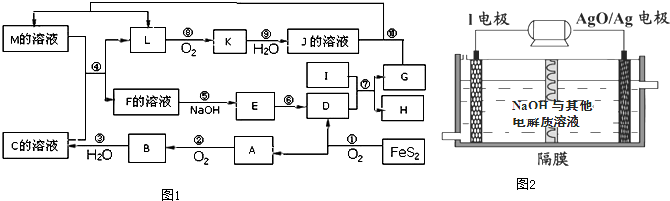
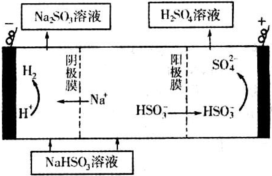 某科研小组为治理SO2对大气的污染,利用烟气中的SO2为原料制取硫酸.
某科研小组为治理SO2对大气的污染,利用烟气中的SO2为原料制取硫酸.