题目内容
15.NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,11.2LC2H5OH含有的氢原子数为3NA | |
| B. | 25℃时,1LpH=12的碳酸钠溶液中含有Na+的数目为0.02NA | |
| C. | 过氧化钠与水反应时,生成0.5molO2转移的电子数为NA | |
| D. | 2molSO2和1molO2在一定条件下充分反应,所得混合气体的分子数等于2NA |
分析 A.标准状况下,乙醇的状态不是气态;
B.碳酸钠溶液中碳酸根离子部分水解生成氢氧根离子,钠离子的物质的量大于碳酸根离子的2倍;
C.Na2O2与H2O的反应2Na2O2+2H2O=4NaOH+O2↑,此反应转移2mol电子,生成1molO2;
D.2molSO2和1molO2在一定条件下充分反应是可逆反应不能进行彻底.
解答 解:A.标况下乙醇不是气体,不能使用标况下的气体摩尔体积计算,故A错误;
B.25℃时,1L pH=12的Na2CO3溶液中含有0.01mol氢氧根离子,碳酸根离子在溶液中部分水解生成氢氧根离子,所以碳酸根离子的物质的量大于0.01mol,钠离子的物质的量大于0.02mol,溶液中含有Na+的数目大于0.02NA,故B错误;
C.Na2O2与H2O的反应是歧化反应:2Na2O2+2H2O=4NaOH+O2↑此反应转移2mol电子,生成1molO2,故当生成0.5molO2,转移电子1mol,数目为NA,故C正确;
D.2molSO2和1molO2在一定条件下充分反应是可逆反应不能进行彻底,所得混合气体的分子数大于2NA,故D错误;
故选C.
点评 本题考查阿伏伽德罗常数的计算与判断,题目难度中等,涉及知识点较多、综合性较强,充分考查学生的分析、理解能力及灵活应用基础知识的能力,注意熟练掌握物质的量与阿伏伽德罗常数、氧化还原反应、可逆反应的分析判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.2016年12月1日国际纯粹与应用化学联合会宣布,将合成的四种新元素命名为113号 (缩写为Nh)、115号(Mc)、117号(Ts)和118号(Og).下列说法正确的是( )
| A. | 113号元素的氧化物为两性氧化物 | |
| B. | 115号元素位于第六周期第VA族 | |
| C. | 117号元素的某种原子,核内含176个中子,此原子是${\;}_{117}^{176}$Ts | |
| D. | 118号元素的原子最外层有8个电子 |
6.下列实验操作正确且能达到实验目的是( )
| A. | 在蒸发皿中加热胆矾晶体制无水硫酸铜 | |
| B. | 用向下排空气法收集NO2气体 | |
| C. | 用K3[Fe(CN)6]溶液检验FeCl2溶液中的Fe2+ | |
| D. | 将CO2与HCl混合气体通过碱石灰可得到纯净的CO2 |
10.标准状况下,下列物质中,其体积最大的是( )
| A. | 44g CO2 | B. | 11.2L H2 | C. | 2mol Fe | D. | 2mol H2O |
20.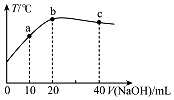 在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
 在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )| A. | 若a点溶液呈酸性,此时:c(CH3COO-)-c(CH3COOH)=2c(H+)-2c(OH-) | |
| B. | B.从a到b:$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$逐渐增大 | |
| C. | 水的电离程度:b点<c点 | |
| D. | 溶液的pH值:a点<c点<b点 |
7.下列离子方程式正确的是( )
| A. | 向Fe2(SO4)3溶液中加入铁粉:Fe3++Fe═2Fe3+ | |
| B. | 石灰石溶于醋酸:CaCO3+2CH3COOH═2CH3COO-+Ca2++CO2↑+H2O | |
| C. | 铜跟浓硝酸反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ |
4.已知HF 酸性强于CH3COOH,常温下有下列三种溶液.有关叙述不正确的是( )
| 编号 | ① | ② | ③ |
| PH | 11 | 3 | 3 |
| 溶液 | NaOH溶液 | CH3COOH溶液 | HF溶液 |
| A. | CH3COOH稀溶液中加入少量CH3COONa,能使比值c(CH3COO-)/c(Na+)增大 | |
| B. | ①、②等体积很合后:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | 向②加入NaF固体,CH3COOH电离平衡正向移动 | |
| D. | 中和相同体积的②、③,需消耗①的体积②<③ |
5.分枝酸可用于生化研究,其结构简式如图.下列关于分枝酸的叙述正确的是( )


| A. | 分子中含有5种官能团 | |
| B. | 可与乙醇、乙酸反应,且反应类型相同 | |
| C. | 1mol分枝酸最多可与3molNaOH发生中和反应 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且反应类型相同 |