题目内容
20.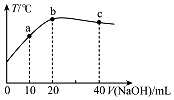 在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )| A. | 若a点溶液呈酸性,此时:c(CH3COO-)-c(CH3COOH)=2c(H+)-2c(OH-) | |
| B. | B.从a到b:$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$逐渐增大 | |
| C. | 水的电离程度:b点<c点 | |
| D. | 溶液的pH值:a点<c点<b点 |
分析 A.a点溶液中溶质为等浓度的醋酸和醋酸钠;
B.a点到b点氢氧化钠增多,氢氧化钠与醋酸恰好中和,醋酸根离子浓度增大,醋酸的浓度减小;
C.b点溶液中溶质为醋酸钠,c点溶液中溶质为醋酸钠和氢氧化钠,醋酸钠促进水的电离,氢氧化钠抑制水的电离;
D.a点溶液中溶质为等浓度的醋酸和醋酸钠,b点溶液中溶质为醋酸钠,c点为等浓度的醋酸钠和氢氧化钠.
解答 解:A.a点溶液中溶质为等浓度的醋酸和醋酸钠,溶液显酸性据电荷守恒有c(Na+)+c(H+)=c(CH3COO-)+c(OH-),据物料守恒有2c(Na+)=c(CH3COO-)+c(CH3COOH),用电荷守恒的2倍-物料守恒得:c(CH3COO-)-c(CH3COOH)=2c(H+)-2c(OH-),故A正确;
B.a点到b点氢氧化钠增多,氢氧化钠与醋酸恰好中和,醋酸根离子浓度增大,醋酸的浓度减小,所以:$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$逐渐减小,故B错误;
C.b点醋酸与氢氧化钠恰好反应生成醋酸钠,醋酸钠水解促进水的电离,c点溶液中溶质为醋酸钠和氢氧化钠,氢氧化钠抑制水的电离,所以水的电离程度:b点>c点,故C错误;
D.a点溶液显酸性,b、c点为碱性,c点溶液碱性更强,所以溶液的pH值:a点<b点<c点,故D错误.
故选A.
点评 本题考查了弱电解质的电离、盐的水解,题目难度中等,侧重于考查学生的分析能力和计算能力,注意把握溶液中的电荷守恒和物料守恒.

练习册系列答案
相关题目
11.下列化学用语表示正确的是( )
| A. | HClO的结构式:H-Cl-O | B. | MgO的电子式:Mg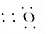 | ||
| C. | 四氯化碳分子比例模型: | D. | 聚四氟乙烯的结构简式: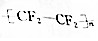 |
8.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 25℃,pH=11的Na2CO3溶液中由水电离出的H+的数目为10-3NA | |
| B. | 标准状况下,2.24L NO与11.2L O2混合后气体的分子数小于NA | |
| C. | 120g熔融的NaHSO4中含阳离子总数为2NA | |
| D. | 用5mL 3mol/L FeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015NA |
15.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2LC2H5OH含有的氢原子数为3NA | |
| B. | 25℃时,1LpH=12的碳酸钠溶液中含有Na+的数目为0.02NA | |
| C. | 过氧化钠与水反应时,生成0.5molO2转移的电子数为NA | |
| D. | 2molSO2和1molO2在一定条件下充分反应,所得混合气体的分子数等于2NA |
9.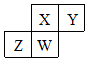 短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,W原子的质子数是其最外层电子数的三倍.下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,W原子的质子数是其最外层电子数的三倍.下列说法不正确的是( )
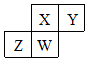 短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,W原子的质子数是其最外层电子数的三倍.下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,W原子的质子数是其最外层电子数的三倍.下列说法不正确的是( )| A. | 元素Y有同素异形体 | |
| B. | 最高价氧化物对应水化物的酸性:X>Z | |
| C. | 简单气态氢化物的热稳定性:Y>Z | |
| D. | 原于半径:W>Z>Y>X |
10.化学在生产和日常生活中有着重要作用,下列有关说法不正确的是( )
| A. | 硅酸钠的水溶液俗称水玻璃,可用作木材防火剂 | |
| B. | “地沟油”禁止食用,但可以用来制肥皂 | |
| C. | 用聚乙烯塑料代替聚乳酸塑料可减少白色污染 | |
| D. | 利用粮食酿酒经过了淀粉→葡糖糖→乙醇的化学变化过程 |

 .
.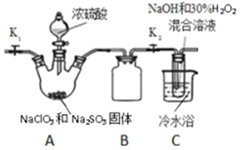 亚氯酸钠(NaClO2)和ClO2都是重要的漂白剂.通常情况下,ClO2是一种具有强氧化性的黄色气体,常用于水的净化和纸浆、纺织品的漂白.ClO2易发生爆炸,在生产、使用时可用其它气体进行稀释.ClO2易与碱反应生成亚氯酸盐和氯酸盐.
亚氯酸钠(NaClO2)和ClO2都是重要的漂白剂.通常情况下,ClO2是一种具有强氧化性的黄色气体,常用于水的净化和纸浆、纺织品的漂白.ClO2易发生爆炸,在生产、使用时可用其它气体进行稀释.ClO2易与碱反应生成亚氯酸盐和氯酸盐.