题目内容
19.下列不能通过单质间反应而制得的物质是( )| A. | CuCl2 | B. | CuO | C. | FeCl2 | D. | HCl |
分析 A.CuCl2可由Cu在Cl2中燃烧生成;
B.铜与氧气反应生成氧化铜;
C.铁和氯气反应生成三氯化铁;
D.氢在氯气中燃烧生成氯化氢.
解答 解:A.Cu在Cl2中燃烧生成CuCl2,Cu+Cl2$\frac{\underline{\;点燃\;}}{\;}$CuCl2,单质间反应能生成,故A不选;
B.铜与氧气反应生成氧化铜,单质间反应能生成,故B不选;
C.铁和氯气反应生成三氯化铁2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,单质间反应不能生成FeCl2,故C选;
D.氢在氯气中燃烧生成氯化氢,单质间反应能生成,故D不选;
故选C.
点评 本题考查了元素化合物的性质,熟悉相关的化学反应的方程式是解答的关键,注意物质的特征反应和基础知识的积累,题目较简单.

练习册系列答案
相关题目
10.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | △H>0表示产物的总能量低于反应物的总能量 | |
| C. | △H 的单位kJ•mol-1,热量Q的单位为kJ | |
| D. | 化学键断裂过程中释放能量 |
7.某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B=H++HB- HB-?H++B2-.在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是( )
| A. | c(B2-)+c(HB-)=0.1 mol/L | B. | c(B2-)+c(HB-)+c(H2B)=0.1 mol/L | ||
| C. | c(OH-)=c(H+)+c(HB-)+2c(H2B) | D. | c(Na+)+c(OH-)=c(H+)+c(HB-) |
14.若1g CO2中含有x个原子,则阿伏加德罗常数可表示为( )
| A. | $\frac{1}{44}$ mol-1 | B. | $\frac{x}{22}$ mol-1 | C. | $\frac{3x}{44}$ mol-1 | D. | $\frac{44x}{3}$ mol-1 |
4.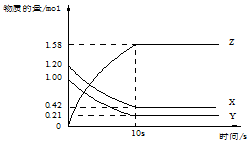 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )| A. | 反应开始到10s,用Z表示的反应速率为0.158mol/(L•s) | |
| B. | 反应开始到10s,X的物质的量浓度减少了0.79mol/L | |
| C. | 反应的化学方程式为:X(g)+Y(g)?Z(g) | |
| D. | 反应开始到10s时,Y的转化率为79.0% |
9.下列化学式及结构式中,从成键情况看不合理的是( )
| A. | 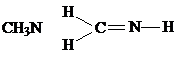 | B. | 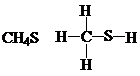 | ||
| C. |  | D. | 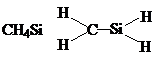 |
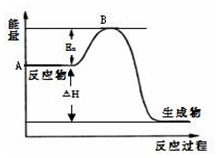 2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:
2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答: