题目内容
11.下列反应中,属于取代反应的是( )①CH3CH═CH2+Br2$\stackrel{CCl_{4}}{→}$CH3CHBrCH2Br
②CH3CH2OH $→_{170℃}^{浓H_{2}SO_{4}}$CH2═CH2↑+H2O
③CH3CH2OH+CH3CH2OH $→_{140℃}^{浓硫酸}$ CH3CH2OCH2CH3+H2O
④C6H6+HNO3$→_{△}^{浓H_{2}SO_{4}}$C6H5NO2+H2O.
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
分析 “有机化合物分子里的某些原子或原子团被其它原子或原子团所代替的反应”为取代反应,据此分析解答.
解答 解:①CH3CH═CH2+Br2$\stackrel{CCl_{4}}{→}$CH3CHBrCH2Br属于加成反应,故错误;
②CH3CH2OH $→_{170℃}^{浓H_{2}SO_{4}}$CH2═CH2↑+H2O属于消去反应,故错误;
③CH3CH2OH+CH3CH2OH $→_{140℃}^{浓硫酸}$ CH3CH2OCH2CH3+H2O属于酯化反应也属于取代反应,故正确;
④C6H6+HNO3$→_{△}^{浓H_{2}SO_{4}}$C6H5NO2+H2O属于取代反应,故正确;
故选B.
点评 本题考查有机化学反应,为高频考点,明确取代反应、消去反应、加成反应概念含义是解本题关键,侧重考查学生分析判断能力,注意:酯化反应、水解反应也属于取代反应.

练习册系列答案
相关题目
2.下列关于能源的说法不正确的是( )
| A. | 通过煤的气化和液化获得洁净的燃料 | |
| B. | 加快核能、太阳能、沼气等新能源的开发利用 | |
| C. | 减少资源消耗,注重资源的重复使用、资源的循环再生 | |
| D. | 大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |
19.下列不能通过单质间反应而制得的物质是( )
| A. | CuCl2 | B. | CuO | C. | FeCl2 | D. | HCl |
6.0.1mol/L氨水溶液在稀释过程中,始终保持增大趋势的是( )
| A. | OH-的物质的量 | B. | c(H+) c(OH-) | C. | c(NH4+) | D. | c(OH-) |
3.下列说法正确的是( )
| A. | 丙烷是直链烃,所以分子中3个碳原子也在一条直线上 | |
| B. | 丙烯所有原子均在同一平面上 | |
| C. | 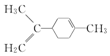 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 | |
| D. |  至少有16个原子共平面,至少8原子共线 至少有16个原子共平面,至少8原子共线 |
4. 节能减排是当下环境保护的重点.
节能减排是当下环境保护的重点.
(1)将C0和气态水通人一个体积固定的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+H20(g)=C02(g)+H2(g)△H<0
800℃,在2L恒容密闭容器中,起始时按照下表数据进行投料,达到平衡状态,K=1.0
①从起始经过5min达到化学平衡时,用生成物C02表示该反应的反应速率v(C02):0.01mol/(L•min)平衡时,容器中C0的转化率为50%
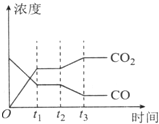
②如图表示上述反应在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况.则t2时刻发生改变的条件可能是降低温度或降低H2浓度或增大H2O(g)浓度(写出一条).
(2)汽车尾气中的一氧化碳是大气污染物,可通过反应:CO(g)+$\frac{1}{2}$02(g)?O2(g)降低其浓度.
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如表所示.请在表中的空格处填写“>”“<”或“=”
②相同温度下,某汽车尾气中C0、C02的浓度分别为1.0X 10-5mol/L和1.0×10-4mol/L.若在汽车的排气管上增加一个补燃器,不断补充02并使其浓度保持为1.0X10-4 mol/L,则最终尾气中CO的浓度为1.1×10-6mol/L(请保留两位有效数字).
(3)CO2在自然界循环时可与CaC03反应,CaC03是一种难溶物质,其Ksp=2.8×10-9.现将等体积的CaCl2溶液与Na2C03溶液混合,若Na2C03溶液的浓度为2×10-4mol/L,则生成 CaC03沉淀所需原CaCl2溶液的最小浓度为5.6×10-5 mol/L.
 节能减排是当下环境保护的重点.
节能减排是当下环境保护的重点.(1)将C0和气态水通人一个体积固定的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+H20(g)=C02(g)+H2(g)△H<0
800℃,在2L恒容密闭容器中,起始时按照下表数据进行投料,达到平衡状态,K=1.0
| H2O | CO | C02 | H2 | |
| n/mol | 0.20 | 0.20 | 0 | 0 |
②如图表示上述反应在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况.则t2时刻发生改变的条件可能是降低温度或降低H2浓度或增大H2O(g)浓度(写出一条).
(2)汽车尾气中的一氧化碳是大气污染物,可通过反应:CO(g)+$\frac{1}{2}$02(g)?O2(g)降低其浓度.
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如表所示.请在表中的空格处填写“>”“<”或“=”
| 容器编号 | c(CO)/mol•L-1 | c(02)/mol•L-1 | c(C02)/mol•L-1 | V(正)和v(逆)比较 |
| Ⅰ | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | V(正)=v(逆 |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 | V(正)> v(逆 |
(3)CO2在自然界循环时可与CaC03反应,CaC03是一种难溶物质,其Ksp=2.8×10-9.现将等体积的CaCl2溶液与Na2C03溶液混合,若Na2C03溶液的浓度为2×10-4mol/L,则生成 CaC03沉淀所需原CaCl2溶液的最小浓度为5.6×10-5 mol/L.

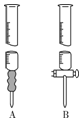 氯化硫酰(SO2Cl2)主要用作氯化剂.它是一种无色液体,熔点-54.1℃,沸点69.1℃.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:
氯化硫酰(SO2Cl2)主要用作氯化剂.它是一种无色液体,熔点-54.1℃,沸点69.1℃.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取: