题目内容
7.某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B=H++HB- HB-?H++B2-.在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是( )| A. | c(B2-)+c(HB-)=0.1 mol/L | B. | c(B2-)+c(HB-)+c(H2B)=0.1 mol/L | ||
| C. | c(OH-)=c(H+)+c(HB-)+2c(H2B) | D. | c(Na+)+c(OH-)=c(H+)+c(HB-) |
分析 该二元酸第一步完全电离、第二步部分电离,所以H2B溶液中存在的微粒有H+、HB-、B2-、OH-,不存在H2B,HB-能发生电离不能发生水解,0.1mol/L的Na2B溶液中存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断.
解答 解:该二元酸第一步完全电离、第二步部分电离,所以H2B溶液中存在的微粒有H+、HB-、B2-、OH-,不存在H2B,HB-能发生电离不能发生水解,
A.溶液中B2-只发生第一步水解,根据物料守恒得c(B2-)+c(HB-)=0.1 mol/L,故A正确;
B.溶液中B2-只发生第一步水解,所以溶液中不存在H2B,故B错误;
C.根据电荷守恒得c(Na+)+c(H+)=c(OH-)+2c(B2-)+c(HB-),根据物料守恒得c(Na+)=2[c(B2-)+c(HB-)],所以得c(HB-)+c(H+)=c(OH-),故C错误;
D.根据C知,c(HB-)+c(H+)=c(OH-),c(Na+)+c(OH-)=c(Na+)+c(HB-)+c(H+)>c(H+)+c(HB-),故D错误;
故选A.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断能力,明确“该二元酸电离特点”是解本题关键,注意:该酸根离子只能发送一步水解,为易错题.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
18.通过以下反应均可获取H2.下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g)△H1=571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g)△H2=131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g)△H3=206.1kJ•mol-1.
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g)△H1=571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g)△H2=131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g)△H3=206.1kJ•mol-1.
| A. | 反应①中电能转化为化学能 | |
| B. | 反应②为放热反应 | |
| C. | 反应③使用催化剂,△H3减小 | |
| D. | 反应②中,反应物的键能大于生成物的键能 |
15.下列有关化学用语表示正确的是( )
| A. | N2的电子式: | B. | S2-的结构示意图: | ||
| C. | HF的电子式: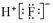 | D. | 肼(N2H4)的结构简式:H2N-NH2 |
2.下列关于能源的说法不正确的是( )
| A. | 通过煤的气化和液化获得洁净的燃料 | |
| B. | 加快核能、太阳能、沼气等新能源的开发利用 | |
| C. | 减少资源消耗,注重资源的重复使用、资源的循环再生 | |
| D. | 大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |
19.下列不能通过单质间反应而制得的物质是( )
| A. | CuCl2 | B. | CuO | C. | FeCl2 | D. | HCl |
17.X、Y、Z、M、N是原子序数依次增大的短周期主族元素,其中X与Z为同族元素,Y和M为同族元素,且Y与M的核外电子数之和为X和Z元素的核外电子数之和的2倍,下列说法正确的是( )
| A. | 原子半径:Z>M>N>X>Y | B. | M与N形成的化合物中N显正价 | ||
| C. | 单质沸点:Z>M>N>Y>X | D. | 最高正价:N>M=Y>Z=X |

 .
.