题目内容
17.将新制氯水注入KI溶液中充分反应后,再加CCl4,振荡后静置,看到的现象是( )| A. | 液体均一,呈紫红色 | |
| B. | 液体分两层,上层为紫红色,下层为无色 | |
| C. | 液体分两层,上层为无色,下层为紫红色 | |
| D. | 液体均一,呈无色 |
分析 氯水加入KI溶液中振荡,发生Cl2+2KI═2KCl+I2,加CCl4,溶液分层,四氯化碳的密度比水大,有色层在下层,以此来解答.
解答 解:少量氯水加入KI溶液中振荡,发生Cl2+2KI═2KCl+I2,加CCl4,生成的碘易溶于四氯化碳,四氯化碳与水不互溶,溶液分层,四氯化碳的密度比水大,有色层在下层,下层为紫红色,
故选C.
点评 本题考查卤素单质的置换反应及萃取,明确氧化性的强弱及萃取、分液中萃取剂的选择、密度等知识即可解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.下列说法中,不正确的是( )
| A. | 用渗析的方法制制氢氧化铁胶体 | |
| B. | SiO2、NaCl、I2、C2H6O均能真实表示物质分子组成 | |
| C. | ${\;}_{8}^{18}$O2-离子结构示意图 | |
| D. | 冰酸酸、铝热剂、硫酸钡、SO2分别屈于酸、混合物、强电解质、非电解质 |
12.短周期元素W、X、Y、Z在元素周期表中的位置如表所示,其中Z的单质,是一种重要半导体材料.广泛应用于电子工业的各个领域.
(1)W在元素周期表中的位位置是第二周期第ⅣA族
(2)Z的原子结构示意图为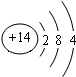
(3)X和Y离子半径最大的是N3-(填离子符号)
(4)下列选项中.能证明元素非佥属性X强于W的是CD
A.原子序数:W>X B.最低化合价:X>W
C.最简单氢化物的稳定性:X>W D.最高价氧化物的水化物酸性:X>W
(5)写出表中Y的最高价氧化物对应水化物的电离方程式Mg(OH)2?Mg2++2OH-
(6)元素周期表中与同Z同期的某金属元素形成的单质A,可发生如图所示的转化
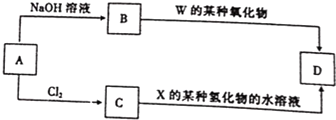
其中化含物D是-种白色沉淀,则生成物B的化学式为NaAlO2,C转化生成D的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
| W | X | ||
| Y | Z |
(2)Z的原子结构示意图为

(3)X和Y离子半径最大的是N3-(填离子符号)
(4)下列选项中.能证明元素非佥属性X强于W的是CD
A.原子序数:W>X B.最低化合价:X>W
C.最简单氢化物的稳定性:X>W D.最高价氧化物的水化物酸性:X>W
(5)写出表中Y的最高价氧化物对应水化物的电离方程式Mg(OH)2?Mg2++2OH-
(6)元素周期表中与同Z同期的某金属元素形成的单质A,可发生如图所示的转化

其中化含物D是-种白色沉淀,则生成物B的化学式为NaAlO2,C转化生成D的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
2.能正确表示下列反应的离子方程式的是( )
| A. | 向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | Na2O2与H2O反应制备O2:2Na2O2+2H2O═4Na++4OH-+O2↑ | |
| D. | 向FeBr2溶液中通入足量氯气:2Fe2++2Br-+3Cl2═2Fe3++Br2+6Cl- |
6.能正确表示下列反应的离子方程式是( )
| A. | 用过量氨水吸收工业尾气中的SO2:2NH3•H20+SO2═2NH4++SO32-+H2O | |
| B. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用铜做电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| D. | 向含有Fe2O3悬浊液中通入HI:Fe2O3+6H+═2Fe3++3H2O |
7. 环己烯是一种重要的化工原料.
环己烯是一种重要的化工原料.
(1)实验室可由环己醇制备环己烯,反应的化学方程式是 .
.
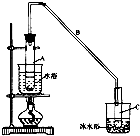
(2)实验装置如下图所示,将10mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.环己醇和环己烯的部分物理性质如下:
①A中碎瓷片的作用是防止暴沸;导管B除了导气外还具有的作用是冷凝.
②试管A置于水浴中的目的是受热均匀,便于控温;
试管C置于冰水浴中的目的是使环己烯液化,减少挥发.
(3)环己烯粗品中含有少量环己醇和酸性杂质.精制环己烯的方法是:
①向环己烯粗品中加入C(填入编号),充分振荡后,分液(填操作名称).
A.Br2的CCl4溶液 B.稀H2SO4 C.Na2CO3溶液
②再对初步除杂后的环己烯进行蒸馏,得到环己烯精品.蒸馏时,蒸馏烧瓶中要加入少量生石灰,目的是除去产品中少量的水.
③实验制得的环己烯精品质量低于理论产量,可能的原因是C.
A.蒸馏时从70℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(4)以下区分环己烯精品和粗品的方法,合理的是B.
A.加入水观察实验现象
B.加入金属钠观察实验现象
C.加入酸性高锰酸钾溶液,振荡后观察实验现象.
 环己烯是一种重要的化工原料.
环己烯是一种重要的化工原料.(1)实验室可由环己醇制备环己烯,反应的化学方程式是
 .
.(2)实验装置如下图所示,将10mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.环己醇和环己烯的部分物理性质如下:
| 密度 (g/cm3) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
②试管A置于水浴中的目的是受热均匀,便于控温;
试管C置于冰水浴中的目的是使环己烯液化,减少挥发.
(3)环己烯粗品中含有少量环己醇和酸性杂质.精制环己烯的方法是:
①向环己烯粗品中加入C(填入编号),充分振荡后,分液(填操作名称).
A.Br2的CCl4溶液 B.稀H2SO4 C.Na2CO3溶液
②再对初步除杂后的环己烯进行蒸馏,得到环己烯精品.蒸馏时,蒸馏烧瓶中要加入少量生石灰,目的是除去产品中少量的水.
③实验制得的环己烯精品质量低于理论产量,可能的原因是C.
A.蒸馏时从70℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(4)以下区分环己烯精品和粗品的方法,合理的是B.
A.加入水观察实验现象
B.加入金属钠观察实验现象
C.加入酸性高锰酸钾溶液,振荡后观察实验现象.