题目内容
3.如果1个12C原子的实际质量为ng,R原子的相对原子质量为M,阿伏加的罗常数用NA表示,则1个R原子的实际质量为:$\frac{nM}{12}$g或$\frac{M}{{N}_{A}}$g.分析 以一个C-12原子质量的$\frac{1}{12}$为标准,其他原子的质量跟它相比较所得到的比,为这种原子的相对原子质量;摩尔质量以g/mol作单位,数值上等于该物质的相对分子质量或相对原子质量,据此进行解答.
解答 解:如果1个12C原子的实际质量为ng,设1个R原子的实际质量为x,则R的相对原子质量为:$\frac{xg}{\frac{1}{12}ng}$=$\frac{12x}{n}$,
R原子的摩尔质量和其相对原子质量数值相等,则$\frac{12x}{n}$=M,整理可得:x=$\frac{nM}{12}$g,
R的摩尔质量为Mg/mol,1molR原子的质量为Mg,则1个R原子的实际质量为:$\frac{Mg}{{N}_{A}}$=$\frac{M}{{N}_{A}}$g,
故答案为:$\frac{nM}{12}$g或$\frac{M}{{N}_{A}}$g.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与其它物理量之间的关系为解答关键,注意掌握摩尔质量与相对原子量之间的关系,试题培养了学生的灵活应用能力.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
14.常温下测得浓度为0.1mol•L-1的下列三种溶液的pH:下列法正确的是( )
| 溶质 | NaHCO3 | Na2CO3 | NaCN |
| pH | 9.7 | 11.6 | 11.1 |
| A. | 阳离子的物质的量浓度之和:Na2CO3>NaCN>NaHCO3 | |
| B. | 相同条件下的酸性:H2CO3<HCN | |
| C. | 三种溶液中均存在电离平衡和水解平衡 | |
| D. | 向0.2 mol•L-1NaHCO3溶液中加入等体积0.1 ol•L-1 NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
11.“84消毒液”能有效杀灭甲型H7N9病毒,某同学参阅“84消毒液”说明中的配方,欲用NaClO固体自己配制480mL含NaClO 25%,密度为1.2g•cm-3的消毒液,下列说法正确的是( )
| A. | 需要称量NaClO固体的质量为144.0 g | |
| B. | 如图所示的仪器中,有四种是不需要的,另外还需一种玻璃仪器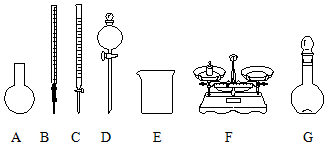 | |
| C. | 配制的溶液在空气中光照,久置后溶液中NaClO的物质的量浓度减小 | |
| D. | 容量瓶用蒸馏水洗净后应烘干才能用于溶液配制,否则结果偏低 |
8.已知:C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-110.35kJ/mol
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H2=-282.57kJ/mol
则C(s)+O2(g)═CO2(g)△H3为( )
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H2=-282.57kJ/mol
则C(s)+O2(g)═CO2(g)△H3为( )
| A. | +172.22kJ/mol | B. | -172.22kJ/mol | C. | -392.92kJ/mol | D. | +392.92kJ/mol |
15.用NA表示阿伏加德罗常数.下列说法正确的是( )
| A. | 标准状况下,7.8g苯中含有的碳碳双键数是0.3NA | |
| B. | 标准状况下,11.2L四氯甲烷所含分子数为0.5NA | |
| C. | 常温常压下,14g乙烯分子中含有的碳碳键数目为2NA | |
| D. | 1mol氢氧根离子(OH-)所含电子数为10NA |
13.以下是侯氏制碱法在实验室进行模拟实验的生产流程示意图,则下列叙述正确的是( )
饱和食盐水$→_{Ⅰ}^{通入足量的气体A}$A和食盐的饱和溶液$→_{Ⅱ}^{通入过量的气体B}$悬浊液$→_{Ⅲ}^{过滤}$晶体$\stackrel{Ⅳ}{→}$纯碱.
饱和食盐水$→_{Ⅰ}^{通入足量的气体A}$A和食盐的饱和溶液$→_{Ⅱ}^{通入过量的气体B}$悬浊液$→_{Ⅲ}^{过滤}$晶体$\stackrel{Ⅳ}{→}$纯碱.
| A. | 第Ⅱ步的离子方程式为Na++NH3.H2O+CO2═NaHCO3↓+NH4+ | |
| B. | 第Ⅲ步得到的晶体是Na2CO3•10H2O | |
| C. | A气体是CO2,B气体是NH3 | |
| D. | 第Ⅳ步操作的主要过程有溶解、蒸发、结晶 |
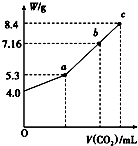 往100mL的NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M,通入CO2的体积(标准状况)与M的质量W的关系如图所示.试回答下列问题:
往100mL的NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M,通入CO2的体积(标准状况)与M的质量W的关系如图所示.试回答下列问题: .
.