题目内容
11.下列关于物质检验的说法正确的是( )| A. | 加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,则原溶液中一定有SO42- | |
| B. | 加入烧碱溶液后加热,产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定有NH4+ | |
| C. | 加入盐酸,放出能使澄清的石灰水变浑浊的无色的气体,则原溶液中一定含有CO32- | |
| D. | 加入AgNO3溶液,有白色沉淀生成,在原溶液中一定含有Cl- |
分析 A.生成的白色沉淀可能为氯化银,不一定含有硫酸根离子;
B.湿润红色石蕊试纸遇碱性物质变蓝,氨气是碱性气体;
C.生成的气体可能为二氧化碳或二氧化硫,原溶液中可能含有碳酸氢根离子、亚硫酸根离子;
D.能使银离子产生白色沉淀的离子有氯离子、硫酸根离子等.
解答 解:A.加入氯化钡溶液后生成的白色沉淀可能为氯化银,原溶液中可能含有银离子,不一定有SO42-,故A错误.
B.湿润红色石蕊试纸遇碱性物质变蓝,加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+,故B正确;
C.加入盐酸,放出能使澄清的石灰水变浑浊的无色的气体,该气体可能为二氧化碳或二氧化硫,原溶液可能含有碳酸氢根离子、亚硫酸根等离子,不一定含有CO32-,故C错误;
D.能使银离子产生白色沉淀的离子有氯离子、CO32-、SO42-等,所以加入AgNO3溶液,有白色沉淀生成,原溶液中不一定有Cl-,故D错误;
故选C.
点评 本题考查了常见离子的检验方法,题目难度中等,明确常见离子的性质为解答关键,注意检验离子存在情况时,必须排除干扰离子,确保检验方案的严密性.

练习册系列答案
相关题目
1.做实验时不小心使皮肤上沾了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸(乙二酸,化学式为H2C2O4)的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为:MnO4-+H2C2O4+H+═CO2↑+Mn2++□(未配平).下列叙述不正确的是( )
| A. | 发生氧化反应的是H2C2O4 | |
| B. | 离子方程式右侧方框内的产物是H2O | |
| C. | 每消耗6 mol H+,转移5 mol电子 | |
| D. | 还原性:Mn2+<H2C2O4 |
19.称取铁粉和氧化铜的混合物6.40g,进行如下实验:
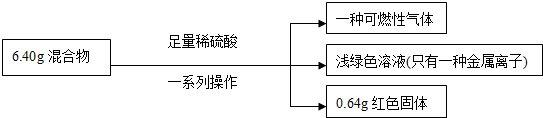
根据实验所得数据,下列说法正确的是( )

根据实验所得数据,下列说法正确的是( )
| A. | 原混合物中铜元素的质量不一定为0.64g | |
| B. | 生成气体体积为2.016L | |
| C. | 实验中反应的硫酸的物质的量为0.1mol | |
| D. | 原混合物中铁的质量分数为87.5% |
6.下列各组物质中所含分子数相同的是( )
| A. | 10g CO和10g N2 | B. | 10g C2H4和10g C3H6 | ||
| C. | 5.6L O2(标准状况)和0.5mol H2O | D. | 224mL He(标准状况)和1.6g CH4 |
3.在Al3++3H2O?Al(OH)3+3H+的平衡体系中,要抑制Al3+的水解,可采取的措施为( )
| A. | 加热 | B. | 加HCl | C. | 加NaOH | D. | 加AlCl3 |
11.淀粉完全水解后的特征是( )
| A. | 能发生银镜反应 | |
| B. | 遇碘水不显兰色 | |
| C. | 与新制Cu(OH)2悬浊液反应,生成红色沉淀 | |
| D. | 有甜味 |
