题目内容
2.(1)FeCl3 的水溶液呈酸(填“酸”“中”或“碱”)性,原因是Fe3++3H2O?Fe(OH)3+3H+(用离子方程式表示):;实验室在配制.FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,以抑制(填“促进”或“抑制”)其水解(2)25°C时,0.1mol•L-1NH4Cl溶液的pH<7(填“<”、“=”或“>”),其原因是NH4++H2O?NH3•H2O+H+(用离子方程式表示);
(3)泡沫灭火器灭火原理Al3++3HCO3-=Al(OH)3↓+3CO2↑(用离子方程式表示)
(4)纯碱可代替洗涤剂洗涤餐具,原因是CO32-+H2O?HCO3-+OH-(用离子方程式表示):.
分析 (1)FeCl3为强酸弱碱盐,铁离子水解而使其溶液呈酸性,为防止其水解,在配制氯化铁溶液时常将FeCl3固体先溶于对应的酸,以抑制其水解;
(2)铵根离子水解显示酸性:NH4++H2O?NH3•H2O+H+;
(3)泡沫灭火器的原理是铝离子和碳酸氢根发生双水解;
(4)纯碱为碳酸钠,水解呈碱性.
解答 解:(1)FeCl3为强酸弱碱盐,铁离子水解而使其溶液呈酸性,水解离子反应方程式为Fe3++3H2O?Fe(OH)3+3H+,根据方程式知,为防止铁离子水解,在配制氯化铁溶液时常将FeCl3固体先溶于稀盐酸中,氢离子浓度增大,从而抑制铁离子水解,故答案为:酸;Fe3++3H2O?Fe(OH)3+3H+;抑制
(2)铵根离子在溶液中水解:NH4++H2O?NH3•H2O+H+,故溶液显酸性,故答案为:<;NH4++H2O?NH3•H2O+H+;
(3)泡沫灭火器原理,离子方程式:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
故答案为:Al3++3HCO3-=Al(OH)3↓+3CO2↑.
(4)纯碱为碳酸钠,水解呈碱性,反应的离子方程式为CO32-+H2O?HCO3-+OH-,故答案为:CO32-+H2O?HCO3-+OH-.
点评 本题考查了盐类水解,根据“谁强谁显性、谁弱谁水解”的规律来分析氯化铁溶液酸碱性,再结合盐类水解的影响因素来分析解答,题目难度不大.

练习册系列答案
相关题目
12.如图是三种有机物的结构简式
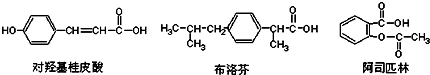
下列说法正确的是( )

下列说法正确的是( )
| A. | 三种有机物都能发生水解反应 | |
| B. | 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 | |
| C. | 三种物质中,其中有两种互为同分异构体 | |
| D. | 三种物质在一定条件下,均可以被氧化反应 |
7.实验室中欲快速制取氢气,最好的方法应该是( )
| A. | 纯锌与稀硫酸 | B. | 粗锌与稀硝酸 | C. | 纯锌与浓硫酸 | D. | 粗锌与稀硫酸 |
11.下列关于物质检验的说法正确的是( )
| A. | 加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,则原溶液中一定有SO42- | |
| B. | 加入烧碱溶液后加热,产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定有NH4+ | |
| C. | 加入盐酸,放出能使澄清的石灰水变浑浊的无色的气体,则原溶液中一定含有CO32- | |
| D. | 加入AgNO3溶液,有白色沉淀生成,在原溶液中一定含有Cl- |
2.化学与生活密切相关,下列说法不正确的是( )
| A. | 碘是人体必需微量元素,所以要多吃富含高碘酸的食物 | |
| B. | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果发生了加成反应 | |
| C. | 食品脱氧剂(含铁粉、氯化钠、炭粉等)的脱氧原理与钢铁的吸氧腐蚀相同 | |
| D. | 加入足量氢氧化钠溶液共热,能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等) |
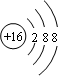 ;32g甲在足量浓硝酸中反应转移的电子数为2NA;甲在足量氧气中充分灼烧的化学方程式为Cu2S+2O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+SO2.
;32g甲在足量浓硝酸中反应转移的电子数为2NA;甲在足量氧气中充分灼烧的化学方程式为Cu2S+2O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+SO2.