题目内容
1.做实验时不小心使皮肤上沾了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸(乙二酸,化学式为H2C2O4)的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为:MnO4-+H2C2O4+H+═CO2↑+Mn2++□(未配平).下列叙述不正确的是( )| A. | 发生氧化反应的是H2C2O4 | |
| B. | 离子方程式右侧方框内的产物是H2O | |
| C. | 每消耗6 mol H+,转移5 mol电子 | |
| D. | 还原性:Mn2+<H2C2O4 |
分析 该反应中Mn元素化合价由+7价变为+2价、C元素化合价由+3价变为+4价,所以高锰酸钾是氧化剂、草酸是还原剂,再结合物质结构、氢离子和转移电子之间的关系式计算.
解答 解:A.该反应中Mn元素化合价由+7价变为+2价、C元素化合价由+3价变为+4价,所以高锰酸钾是氧化剂、草酸是还原剂,则发生氧化反应的是H2C2O4,故A正确;
B.该反应是在酸性条件下的反应,所以生成物中应该是水,故B正确;
C.反应2MnO4-+5H2C2O4+6H+═10CO2↑+2Mn2++8H2O,每消耗6 mol H+,转移电子的物质的量10mol,故C错误;
D.H2C2O4作还原剂,则还原性:Mn2+<H2C2O4,故D正确;
故选C.
点评 本题考查了氧化还原反应,根据元素化合价变化结合基本概念来分析解答,知道乙二酸的结构,注意该反应的条件,题目难度不大.

练习册系列答案
相关题目
12.如图是三种有机物的结构简式
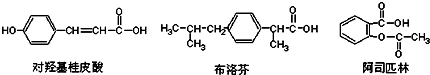
下列说法正确的是( )

下列说法正确的是( )
| A. | 三种有机物都能发生水解反应 | |
| B. | 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 | |
| C. | 三种物质中,其中有两种互为同分异构体 | |
| D. | 三种物质在一定条件下,均可以被氧化反应 |
9.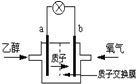 2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200°C左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意如图,下列说法不正确的是( )
2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200°C左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意如图,下列说法不正确的是( )
 2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200°C左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意如图,下列说法不正确的是( )
2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200°C左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意如图,下列说法不正确的是( )| A. | 电池工作时,1mol乙醇被氧化时就有6mol电子转移 | |
| B. | a极为电池的负极 | |
| C. | 电池工作时电流由b极沿导线经灯泡再到a极 | |
| D. | 电池正极的电极反应为:4H++O2+4e-═2H2O |
16.下列实验现象,与新制氯水中的某些成分(括号内物质)没有直接关系的是( )
| A. | 向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,溶液呈红色(Cl2) | |
| B. | 新制氯水使红色布条褪色(Cl2) | |
| C. | 将AgNO3溶液滴加到新制氯水中,有白色沉淀产生(Cl-) | |
| D. | 向NaHCO3固体中加入新制的氯水,有无色气泡产生(H+) |
6.将50mL2mol•L-1的NaCl溶液加水稀释成1mol•L-1的NaCl溶液时,稀释后溶液的体积为( )
| A. | 100mL | B. | 200mL | C. | 150mL | D. | 50mL |
11.下列关于物质检验的说法正确的是( )
| A. | 加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,则原溶液中一定有SO42- | |
| B. | 加入烧碱溶液后加热,产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定有NH4+ | |
| C. | 加入盐酸,放出能使澄清的石灰水变浑浊的无色的气体,则原溶液中一定含有CO32- | |
| D. | 加入AgNO3溶液,有白色沉淀生成,在原溶液中一定含有Cl- |
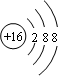 ;32g甲在足量浓硝酸中反应转移的电子数为2NA;甲在足量氧气中充分灼烧的化学方程式为Cu2S+2O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+SO2.
;32g甲在足量浓硝酸中反应转移的电子数为2NA;甲在足量氧气中充分灼烧的化学方程式为Cu2S+2O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+SO2.