题目内容
2.分子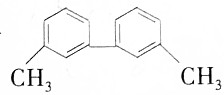 中,在同一平面上的碳原子最少有9个,最多有14个.
中,在同一平面上的碳原子最少有9个,最多有14个.
分析 由结构简式可知,分子中含2个苯环,苯环为平面结构,直接与苯环相连的原子与苯环在同一平面内,结合对称性分析.
解答 解:甲基与苯环平面结构通过单键相连,甲基的C原子处于苯的H原子位置,所以处于苯环这个平面;
两个苯环相连,与苯环相连的碳原子处于该苯环中的H原子位置,也处于另一个苯环这个平面,另一苯环所用的C原子都处于同一平面上,处于苯环对位上的碳原子以及碳原子所连的氢原子共线,所以至少有9个碳原子共面,至多有14个碳原子共面;
故答案为:9;14.
点评 本题考查有机物的结构,注意苯环对位上的碳原子以及碳原子所连的氢原子共线,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1mol C12通入足量NaOH溶液中,转移电子数为NA | |
| B. | 18g D2O含有的中子数为10NA | |
| C. | 0.1mol/L的Na2CO3溶液含CO32-数目为0.1NA | |
| D. | 已知白磷(P4)分子结构为正四面体,则1mol P4含共价键数为4NA |
13.下列说法不正确的是( )
| A. | 麦芽糖及其水解产物均能发生银镜反应 | |
| B. | 饱和硫酸铵和醋酸铅溶液均能使鸡蛋清溶液发生变性 | |
| C. | 油脂、二肽发生水解反应均可能得到含羧基的物质 | |
| D. | 天然橡胶 和杜仲胶 和杜仲胶 的单体是同种物质 的单体是同种物质 |
10.T℃时,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),发生反应:2SO2(g)+O2(g)?2SO3(g),5min时甲达到平衡.其起始量及SO2的平衡转化率如表所示.下列叙述不正确的是( )
| 容器 | 甲 | 乙 | 丙 | |
| 起始量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率 | 80% | α1 | α2 | |
| A. | 0~5min内,甲中SO2的反应速率为0.032mol•L-1•min-1 | |
| B. | T℃时,该反应的平衡常数K=400 | |
| C. | 平衡时,SO2的转化率:α1<80%<α2 | |
| D. | 平衡时,丙中气体平均相对分子质量与甲相同 |
17.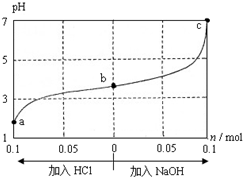 25℃时,将1.0L w mol•L-1 CH3COOH溶液与0.1mol NaOH固体混合,充分反应后向混合液中通(加)入HCl气体或NaOH固体,溶液pH随加入HCl或NaOH的物质的量而变化如图.下列叙述正确的是( )
25℃时,将1.0L w mol•L-1 CH3COOH溶液与0.1mol NaOH固体混合,充分反应后向混合液中通(加)入HCl气体或NaOH固体,溶液pH随加入HCl或NaOH的物质的量而变化如图.下列叙述正确的是( )
 25℃时,将1.0L w mol•L-1 CH3COOH溶液与0.1mol NaOH固体混合,充分反应后向混合液中通(加)入HCl气体或NaOH固体,溶液pH随加入HCl或NaOH的物质的量而变化如图.下列叙述正确的是( )
25℃时,将1.0L w mol•L-1 CH3COOH溶液与0.1mol NaOH固体混合,充分反应后向混合液中通(加)入HCl气体或NaOH固体,溶液pH随加入HCl或NaOH的物质的量而变化如图.下列叙述正确的是( )| A. | a、b、c 对应的混合液中,水的电离程度由大到小的顺序的是a>b>c | |
| B. | c点混合液中c(Na+)>c(CH3COO-) | |
| C. | a、b、c三点都有c(CH3COO-)+c(OH-)=c(Na+)+c(H+) | |
| D. | 若忽略体积变化,则25℃时CH3COOH的电离平衡常数 K=$\frac{0.2}{w-0.2}$×10-7 mol•L-1 |
7.化学科学、技术、社会、环境密切相关.下列说法不正确的是( )
| A. | 利用蓝绿藻等低等生物和微生物在阳光作用下使水分解产生氢气,该方法符合绿色化学原则 | |
| B. | 12C、13C和14C互为同位素,它们的放射性可用于考古断代,可测定生物体死亡的年代 | |
| C. | 食品脱氧剂(含铁粉、氯化钠、炭粉等)的脱氧原理与钢铁的吸氧腐蚀相同 | |
| D. | 利用生物方法脱除生活污水中的氮和磷,防止水体富营养化 |
下列实验操作能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 除去CO中少量的CO2 | 通过足量灼热CuO |
B | 除去CuCO3溶液中的少量 CuO | 加入足量稀H2SO4后,过滤 |
C | 鉴别澄清石灰水和NaOH溶液 | 加入稀HCl |
D | 鉴别硬水和软水 | 加入肥皂水 |
3.(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;
反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2;
在不同温度时K1、K2的值如表:
①反应CO2(g)+H2(g)?CO(g)+H2O(g)△H,平衡常数为K,则△H==△H1-△H2(用△H1和△H2表示),K=$\frac{{K}_{1}}{{K}_{2}}$(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)?CO(g)+H2O(g)是吸热反应(填“吸热”或“放热”).
②能判断CO2(g)+H2(g)?CO(g)+H2O(g)达到化学平衡状态的依据是BC(填序号).
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.将体积比为1:2的CO2、H2气体置于密闭容器中发生上述反应,CO和H2O的体积比保持不变时.
反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2;
在不同温度时K1、K2的值如表:
| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
②能判断CO2(g)+H2(g)?CO(g)+H2O(g)达到化学平衡状态的依据是BC(填序号).
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.将体积比为1:2的CO2、H2气体置于密闭容器中发生上述反应,CO和H2O的体积比保持不变时.
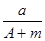 (A-N+m)mol B.
(A-N+m)mol B. 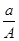 (A-N)mol
(A-N)mol