题目内容
15.温度一定时,在密闭容器中发生可逆反应:mA(s)+nB(g)?pC(g),达到平衡后,若将混合气体的体积压缩到原来的$\frac{1}{2}$,当再次达到平衡时,C的浓度为原平衡时C的浓度的1.9倍,则下列叙述中正确的是( )| A. | m+n<p | B. | C气体的体积分数增大 | ||
| C. | 平衡向正反应方向移动 | D. | B的转化率减小 |
分析 将体积压缩到原来的1/2,C的浓度为原平衡时C的浓度的1.9倍,说明增大压强平衡向逆反应方向移动,据此分析.
解答 解:增大压强平衡向逆反应方向移动,即向气体体积减小的方向移动,由于A是固体,则有n<p,故A错误;C气体的体积分数减小,故B错误;气体B的转化率减小,故C错误、D正确,故选:D.
点评 本题考查化学平衡的影响因素及化学平衡的计算,题目难度不大.

练习册系列答案
相关题目
5.A、B、X、Y、Z、W六种短周期主族元素,A是地壳中含量最多的金属元素,短周期主族元素中B的原子半径最大,X、Y、Z、W元素在周期表中的相对位置如图所示,其中Z元素原子最外层电子数是电子层数的2倍.请回答下列问题:
(1)W的最高价氧化物化学式是Cl2O7;Z 的原子结构示意图为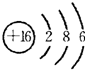 .
.
(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O.
(3)AW3可用于净水,其原理是Al3++3H2O?Al(OH)3(胶体)+3H+.(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应.下列措施中既能提高反应速率,又能提高原料转化率的是d.
a.升高温度 b.加入催化剂
c.将 X的简单气态氢化物及时移离 d.增大反应体系的压强
(5)标准状况下,2.24 L X的简单气态氢化物被200 mL 1 mol•L-1 X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)c(NO3-)>c(H+)>c(NH4+)>c(OH-).
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用 WY2(沸点9.9℃)氧化除去CN-的离子方程式2ClO2+2CN-═N2+2CO2+2Cl-.
| X | Y | |
| Z | W |
 .
.(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O.
(3)AW3可用于净水,其原理是Al3++3H2O?Al(OH)3(胶体)+3H+.(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应.下列措施中既能提高反应速率,又能提高原料转化率的是d.
a.升高温度 b.加入催化剂
c.将 X的简单气态氢化物及时移离 d.增大反应体系的压强
(5)标准状况下,2.24 L X的简单气态氢化物被200 mL 1 mol•L-1 X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)c(NO3-)>c(H+)>c(NH4+)>c(OH-).
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用 WY2(沸点9.9℃)氧化除去CN-的离子方程式2ClO2+2CN-═N2+2CO2+2Cl-.
6.下列溶液中Cl-的物质的量最大的是( )
| A. | 10 mL 0.1 mol•L-1的AlCl3溶液 | B. | 20 mL 0.1 mol•L-1的CaCl2溶液 | ||
| C. | 30 mL 0.2 mol•L-1的KCl溶液 | D. | 100 mL 0.25 mol•L-1的NaCl溶液 |
3.葡萄糖酸钙是一种可促进骨骼生长的营养物质.葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O-→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7+CaCO3-→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
实验流程如下:
(1)第①步中溴水氧化葡萄糖时,下列装置中最适合的是B.
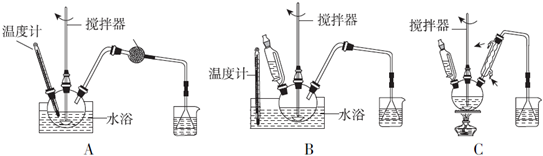
制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是C.
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是提高葡萄糖酸的转化率;本实验中不宜用CaCl2替代CaCO3,理由是氯化钙难以与葡萄糖酸直接反应得到葡萄糖酸钙.
(3)第③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤会损失产品.
(4)第④步加入乙醇的作用是可降低葡萄糖酸钙在溶剂中的溶解度,有利于葡萄糖酸钙的析出.
(5)第⑥步中,下列洗涤剂最合适的是D.
A.冷水 B.热水 C.乙醇 D.乙醇水混合溶液.
C6H12O6(葡萄糖)+Br2+H2O-→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7+CaCO3-→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |

(1)第①步中溴水氧化葡萄糖时,下列装置中最适合的是B.

制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是C.
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是提高葡萄糖酸的转化率;本实验中不宜用CaCl2替代CaCO3,理由是氯化钙难以与葡萄糖酸直接反应得到葡萄糖酸钙.
(3)第③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤会损失产品.
(4)第④步加入乙醇的作用是可降低葡萄糖酸钙在溶剂中的溶解度,有利于葡萄糖酸钙的析出.
(5)第⑥步中,下列洗涤剂最合适的是D.
A.冷水 B.热水 C.乙醇 D.乙醇水混合溶液.
20.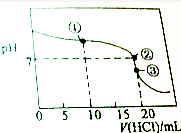 常温下,用0.1000mol•L-1的盐酸滴定20.00mL未知浓度的氨水,滴定曲线如图所示,滴加20.00mL盐酸时所得溶液中,c(Cl-)=c(NH4+)+c(NH3•H2O)+c(NH3),下列说法错误的是( )
常温下,用0.1000mol•L-1的盐酸滴定20.00mL未知浓度的氨水,滴定曲线如图所示,滴加20.00mL盐酸时所得溶液中,c(Cl-)=c(NH4+)+c(NH3•H2O)+c(NH3),下列说法错误的是( )
 常温下,用0.1000mol•L-1的盐酸滴定20.00mL未知浓度的氨水,滴定曲线如图所示,滴加20.00mL盐酸时所得溶液中,c(Cl-)=c(NH4+)+c(NH3•H2O)+c(NH3),下列说法错误的是( )
常温下,用0.1000mol•L-1的盐酸滴定20.00mL未知浓度的氨水,滴定曲线如图所示,滴加20.00mL盐酸时所得溶液中,c(Cl-)=c(NH4+)+c(NH3•H2O)+c(NH3),下列说法错误的是( )| A. | 该氨水的浓度0.1000mol•L-1 | |
| B. | 点①溶液中c(NH4+)+c(NH3•H2O)+c(NH3)=2c(Cl-) | |
| C. | 点②溶液中c(NH4+)=c(Cl-) | |
| D. | 点③溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
17.短周期中的A、B、C、D、E五种元素,原子序数依次增大,A和D,C和E分别同主族,A为短周期元素中原子半径最小的元素,且A与B的原子序数之和等于C的原子序数,C2-与D+的核外电子数相等.则下列说法正确的是( )
| A. | B与A只能组成BA3化合物 | |
| B. | 第三周期中,D原子的原子半径最大 | |
| C. | A、B、C三元素不可能形成离子化合物 | |
| D. | E的氧化物对应水化物一定有强的氧化性 |
18.A、B、C、D为四种短周期元素,已知A、C同主族,B、C、D同周期;A的气态氢化物比C的气态氢化物稳定;B的阳离子比D的阳离子氧化性强;B的阳离子比C的阴离子少一个电子层.下列叙述正确的是( )
| A. | 原子序数:A>C>B>D | B. | 原子半径:B>D>C>A | ||
| C. | 原子序数:C>B>D>A | D. | 简单离子半径:D>B>C>A |