题目内容
6.下列溶液中Cl-的物质的量最大的是( )| A. | 10 mL 0.1 mol•L-1的AlCl3溶液 | B. | 20 mL 0.1 mol•L-1的CaCl2溶液 | ||
| C. | 30 mL 0.2 mol•L-1的KCl溶液 | D. | 100 mL 0.25 mol•L-1的NaCl溶液 |
分析 Cl-的物质的量等于溶液体积、浓度及分子内Cl-的个数的乘积,据此分析解答.
解答 解:A.氯化铝在水溶液中完全电离,该溶液中n(Cl-)=0.1mol/L×3×0.01L=0.003mol;
B.该溶液中n(Cl-)=0.1mol/L×2×0.02=0.004mol;
C.该溶液中n(Cl-)=0.2mol/L×1×0.03L=0.006mol;
D.该溶液中n(Cl-)=0.25mol/L×1×0.1L=0.025mol;
通过以上分析知,氯离子物质的量最大的是D,
故选D.
点评 本题考查物质的量的有关计算,为高频考点,侧重考查学生分析判断及计算能力,明确溶质性质及氯离子物质的量多少影响因素是解本题关键,题目难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
17.下列过程或现象与盐类水解无关的是( )
| A. | 纯碱溶液去油污 | B. | 明矾可作净水剂 | ||
| C. | 加热氯化铁溶液颜色变深 | D. | 硫酸氢钠溶液显酸性 |
14.已知反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)?2CO2(g)+S(l)△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
| A. | 平衡前,充入氮气,容器内压强增大,反应速率加快 | |
| B. | 平衡时,其他条件不变,分离出硫,逆反应速率减小 | |
| C. | 平衡时,其他条件不变,升高温度可提高 SO2 的转化率 | |
| D. | 其他条件不变,缩小容器体积,平衡正反应方向移动,该反应的平衡常数不变 |
1.1molX气体跟amolY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)?bZ(g) 反应达到平衡后,测得X的转化率为50%.而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的$\frac{3}{4}$,则a和b的数值可能是( )
| A. | a=1,b=2 | B. | a=2,b=1 | C. | a=2,b=2 | D. | a=3,b=2 |
18.A、B、C、D、E为原子序数依次增大的短周期主族元素,A与C、B与D分别同主族,且A、C元素的质子数之和是B、D元素质子数之和的一半.下列判断正确的是( )
| A. | 原子半径大小顺序:D>C>B>A | |
| B. | 由B和C元素组成的化合物,可以既含有离子键,又含有共价键 | |
| C. | 元素B、D、E分别与A形成的化合物中,熔沸点最低的是B与A形成的化合物 | |
| D. | 元素D与C形成的化合物在空气中长期放置不易变质 |
15.温度一定时,在密闭容器中发生可逆反应:mA(s)+nB(g)?pC(g),达到平衡后,若将混合气体的体积压缩到原来的$\frac{1}{2}$,当再次达到平衡时,C的浓度为原平衡时C的浓度的1.9倍,则下列叙述中正确的是( )
| A. | m+n<p | B. | C气体的体积分数增大 | ||
| C. | 平衡向正反应方向移动 | D. | B的转化率减小 |
9.下列装置图及有关说法正确的是( )
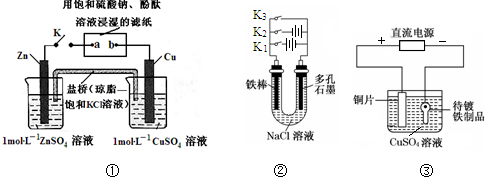

| A. | 装置①中K键闭合时,片刻后可观察到滤纸a点变红色 | |
| B. | 装置①中K键闭合时,片刻后CuSO4溶液中c(Cl-)增大 | |
| C. | 装置②中铁腐蚀的速度由大到小的顺序是:只闭合K1>只闭合K3>只闭合K2>都断开 | |
| D. | 装置③中当铁制品上析出1.6 g铜时,电源负极输出的电子数为0.025 NA |