题目内容
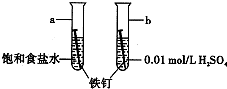 如图是研究铁钉腐蚀的装置图.下列说法不正确的是( )
如图是研究铁钉腐蚀的装置图.下列说法不正确的是( )| A、ab在两处的腐蚀速率a<b |
| B、a、b两处铁钉中的碳均为正极 |
| C、a、b两处铁钉中的铁均失电子被氧化 |
| D、a、b两处的正极反应式均为O2+4e-+4H+═2H2O |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:a中电解质溶液显中性,为铁钉的吸氧腐蚀,b中电解质溶液为稀硫酸,显酸性为析氢腐蚀;
A、硫酸中氢离子浓度较大,电池反应较快,饱和食盐水中氧气的浓度较小,电池反应较慢;
B、a、b中C为原电池的正极;
C、a、b中Fe失电子为原电池的负极;
D、a中正极上氧气的得电子,b中正极上氢离子得电子.
A、硫酸中氢离子浓度较大,电池反应较快,饱和食盐水中氧气的浓度较小,电池反应较慢;
B、a、b中C为原电池的正极;
C、a、b中Fe失电子为原电池的负极;
D、a中正极上氧气的得电子,b中正极上氢离子得电子.
解答:
解:a中电解质溶液显中性,为铁钉的吸氧腐蚀,b中电解质溶液为稀硫酸,显酸性为析氢腐蚀;
A、硫酸中氢离子浓度较大,电池反应较快,饱和食盐水中氧气的浓度较小,电池反应较慢,所以ab在两处的腐蚀速率a<b,故A正确;
B、a中C为原电池的正极,正极上氧气得电子,b中C为原电池的正极,正极上氢离子得电子,故B正确;
C、原电池中失电子的一极为负极,a、b中Fe失电子为原电池的负极,故C正确;
D、a中正极上氧气得电子,其电极反应式为O2+4e-+2H2O═4OH-,b中正极上氢离子得电子,其电极反应式为2H++2e-=H2↑,故D错误;
故选D.
A、硫酸中氢离子浓度较大,电池反应较快,饱和食盐水中氧气的浓度较小,电池反应较慢,所以ab在两处的腐蚀速率a<b,故A正确;
B、a中C为原电池的正极,正极上氧气得电子,b中C为原电池的正极,正极上氢离子得电子,故B正确;
C、原电池中失电子的一极为负极,a、b中Fe失电子为原电池的负极,故C正确;
D、a中正极上氧气得电子,其电极反应式为O2+4e-+2H2O═4OH-,b中正极上氢离子得电子,其电极反应式为2H++2e-=H2↑,故D错误;
故选D.
点评:本题考查了金属的腐蚀,试管内电解质溶液的酸碱性来确定铁发生腐蚀类型,再结合发生析氢腐蚀和吸氧腐蚀的原理来分析解答,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混台后所得溶液的pH如下表:
下列判断不正确的是( )
| 实验编号 | HA物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液的pH |
| ①②③ | 0.1 | 0.1 | pH=9 |
| C | 0.2 | pH=7 | |
| 0.2 | 0.1 | pH<7 |
| A、HA的电离方程式为:HA?H++A- |
| B、不考虑其他组的实验结果,c≥0.2 |
| C、③组实验中,混合溶液中c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-) |
| D、①组实验中,混合溶液中c(A-)=(0.1+10-9-10-5)mol/L |
下列比较中,正确的是( )
| A、CH4与SiH4的稳定性:CH4>SiH4 |
| B、HClO与H2SO4的酸性:HClO>H2SO4 |
| C、1mol HCl(g)的能量比1mol H2(g)和1mol Cl2(g)的能量和高 |
| D、Cl与S的原子半径:Cl>S |
下列说法正确的是( )
| A、甲苯是饱和烃,氯乙烯是不饱和烃 |
| B、石油的裂化产品能使溴水褪色 |
| C、蛋白质在CuSO4溶液中发生盐析 |
| D、油脂在NaOH溶液中水解生成高级脂肪酸和甘油 |
设表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A、22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| B、常温下,1L O.1mol/L NH4NO3的溶液中含氮原子数为0.2NA |
| C、室温下,21.Og乙烯和丁烯的混合气体中含有的碳原子数目为NA |
| D、含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol/L |
下列与有机物的结构、性质有关的叙述正确的是( )
| A、用新制氢氧化铜悬浊液无法鉴别葡萄糖和乙酸 |
| B、乙酸与乙醇可以发生酯化反应,又均可与碳酸氢钠溶液反应 |
| C、硫酸铵、硫酸铜和乙醇均能使蛋白质变性 |
| D、二氯甲烷不存在同分异构体 |
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4L SO3中含有的氧原子数为3NA |
| B、标准状况下,22.4L Cl2与足量的稀NaOH 溶液反应,转移电子总数为2NA |
| C、1mol N5+共有34NA核外电子 |
| D、0.5mol CCl4中含有共价键数目为4NA |
下列说法中不正确的是( )
| A、高吸水性树脂属于功能高分子材料 |
| B、SiC、Al2O3的熔点很高,可用作高温结构陶瓷 |
| C、光导纤维、合成纤维和人造纤维都是有机高分子化合物 |
| D、合金拓展了金属材料的使用范围,合金中也可能含有非金属元素 |