题目内容
20.硫化氢分解制取氢气和硫磺的原理为:2H2S(g)?S2(g)+2H2(g),在2.0L恒容密闭容器中充入0.1molH2S,不同温度下测得H2S的转化率与时间的关系如下图所示.下列说法正确的是( )
| A. | 正反应为放热反应 | |
| B. | 图中P点:v(正)>v(逆) | |
| C. | 950℃时,0~1.25s生成H2的平均反应速率为:0.016mol•L-1•s-1 | |
| D. | 950℃时,该反应的平衡常数的值小于3.125×10-4 |
分析 A、升高温度,硫化氢的转化率变大,说明平衡正向移动;
B、图中P点未达平衡状态,在这种状态下最终达平衡状态,硫化氢的转化率变大;
C、H2的平均反应速率为:v=$\frac{△c}{△t}$;
D、Qc=$\frac{0.0{1}^{2}×0.05}{0.0{4}^{2}}$=3.125×10-4,而反应正向移动,所以平衡常数的值大于3.125×10-4.
解答 解:A、升高温度,硫化氢的转化率变大,说明平衡正向移动,正反应方向是吸热反应,故A错误;
B、图中P点未达平衡状态,在这种状态下最终达平衡状态,硫化氢的转化率变大,反应向正反应方向进行,所以v(正)>v(逆),故B正确;
C、2H2S(g)?S2(g)+2H2(g),在2.0L恒容密闭容器中充入0.1molH2S,此时硫化氢的转化率为:20%,则氢气的变化量为:0.1×0.2=0.02mol,所以v(H2)=$\frac{\frac{0.02mol}{2L}}{1.25s}$=0.008mol•L-1•s-1,故C错误;
D、Qc=$\frac{0.0{1}^{2}×0.05}{0.0{4}^{2}}$=3.125×10-4,而反应正向移动,所以平衡常数的值大于3.125×10-4,故D错误;
故选B.
点评 本题考查化学平衡的计算等知识,题目难度中等,注意掌握化学反应速率、明确反应进行的方向,是解题的关键.

练习册系列答案
相关题目
10.化学概念在逻辑上存在如图所示关系,对下列概念的说法正确的是( )

| A. | 溶液与胶体属于包含关系 | |
| B. | 化合物与氧化物属于包含关系 | |
| C. | 电解质与化合物属于交叉关系 | |
| D. | 氧化还原反应与化合反应属于并列关系 |
11.下列过程所涉及到的反应不会出现氧化还原反应的是( )
| A. | 金属钠久置于空气中,先变暗,再变白,又“出汗”,最后变成白色固体 | |
| B. | 由海水制备金属镁和游离态的溴 | |
| C. | 工业上用石灰石、石英、纯碱制玻璃 | |
| D. | 高温下用二氧化硅和碳反应制备粗硅 |
15.将蔗糖水解,并用新制的氢氧化铜悬浊液检验其水解产物的实验中,要进行的主要操作是( )
①加热
②滴入稀硫酸
③加入新制的氢氧化铜悬浊液
④加入适量的氢氧化钠溶液调节至碱性.
①加热
②滴入稀硫酸
③加入新制的氢氧化铜悬浊液
④加入适量的氢氧化钠溶液调节至碱性.
| A. | ①→②→③→④→① | B. | ②→①→④→③→① | C. | ②→④→①→③→① | D. | ③→④→①→②→① |
5.下列物质的鉴别方法不正确的是( )
| A. | 用氯化钙溶液鉴别Na2CO3和NaHCO3两种溶液 | |
| B. | 用氢氧化钠溶液鉴别MgCl2溶液、AlCl3溶液 | |
| C. | 利用丁达尔效应鉴别Fe(OH)3胶体与FeCl3溶液 | |
| D. | 用焰色反应鉴别NaCl、KCl和Na2SO4 |
9.将一定量的钠铝合金置于水中,合金全部溶解,得到20mL c(OH-)=1mol/L的溶液,然后向溶液中滴加l mol•L-1的盐酸至沉淀质量最大时,消耗盐酸40mL,原合金中钠的质量为( )
| A. | 0.46g | B. | 0.69g | C. | 0.92g | D. | 0.23g |
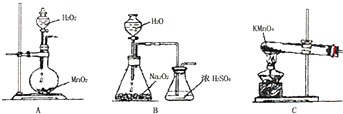
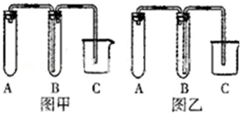 化学是一门以实验为基础的学科.
化学是一门以实验为基础的学科.