题目内容
15.将蔗糖水解,并用新制的氢氧化铜悬浊液检验其水解产物的实验中,要进行的主要操作是( )①加热
②滴入稀硫酸
③加入新制的氢氧化铜悬浊液
④加入适量的氢氧化钠溶液调节至碱性.
| A. | ①→②→③→④→① | B. | ②→①→④→③→① | C. | ②→④→①→③→① | D. | ③→④→①→②→① |
分析 蔗糖水解生成葡萄糖,根据葡萄糖与新制Cu(OH)2悬浊液发生反应需在碱性的条件下进行,结合实验操作步骤中的注意点选择先后顺序,即可进行解答.
解答 解:蔗糖水解的实验步骤为:取少量其水解产物中加入3~5滴稀硫酸选②;将混合液煮沸几分钟选①;
检验其水解产物的实验步骤为:因还原性糖葡萄糖与新制Cu(OH)2悬浊液发生氧化反应,须在碱性条件下,而此时溶液中有硫酸呈酸性,所以,在冷却后的溶液中加入新制Cu(OH)2悬浊液溶液前,加碱中和至碱性所以选④;加入新制Cu(OH)2悬浊液溶液选③;加热选①;其实验结果有砖红色沉淀产生证明蔗糖已经水解,
所以该实验中操作步骤的排列正确顺序为:②①④③①,
故选B.
点评 本题考查了蔗糖的水解及其产物葡萄糖与新制Cu(OH)2悬浊液作用的实验,掌握葡萄糖与新制Cu(OH)2悬浊液反应的条件是解答的关键,注意根据操作的要点选择操作顺序,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.在某无色透明的酸性溶液中,能大量共存的离子组是( )
| A. | Ba2+、K+、SO42-、HCO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | Na+、K+、Cl-、NO3- | D. | Fe3+、Ag+、SO42-、Cl- |
6.设NA代表阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 常温常压下,8g甲烷(12CH4)所含的中子数为5NA | |
| B. | 64g的铜发生氧化还原反应,一定失去2NA个电子 | |
| C. | 常温常压下,0.5 mol•L-1的乙酸溶液中,乙酸的分子数目略小于0.05NA | |
| D. | 标准状况下,22.4L 氧单质中氧原子数可能为2.5NA |
3.金属及其化合物转化关系是化学学习的重要内容之一.下列各组物质的转化关系中不能全部通过一步反应完成的是( )
| A. | Al→Al2O3→Al(OH)3→AlCl3 | B. | Fe→FeCl3→Fe(OH)3→Fe2O3 | ||
| C. | Mg→MgCl2→Mg(OH)2→MgSO4 | D. | Na→NaOH→Na2CO3→NaCl |
20.硫化氢分解制取氢气和硫磺的原理为:2H2S(g)?S2(g)+2H2(g),在2.0L恒容密闭容器中充入0.1molH2S,不同温度下测得H2S的转化率与时间的关系如下图所示.下列说法正确的是( )


| A. | 正反应为放热反应 | |
| B. | 图中P点:v(正)>v(逆) | |
| C. | 950℃时,0~1.25s生成H2的平均反应速率为:0.016mol•L-1•s-1 | |
| D. | 950℃时,该反应的平衡常数的值小于3.125×10-4 |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.0gH218O与D20的混合物中所含中子数为NA | |
| B. | 等物质的量的水与重水含有的中子数相等 | |
| C. | 18gD20和18gH20中含有的质子数均为10NA | |
| D. | 235g核素$\left.\begin{array}{l}{235}\\{92}\end{array}\right.$U发生裂变反应:$\left.\begin{array}{l}{235}\\{92}\end{array}\right.$U+$\left.\begin{array}{l}{1}\\{0}\end{array}\right.$n$\frac{\underline{\;裂变\;}}{\;}$$\left.\begin{array}{l}{90}\\{38}\end{array}\right.$Sr+$\left.\begin{array}{l}{136}\\{54}\end{array}\right.$U+10$\left.\begin{array}{l}{1}\\{0}\end{array}\right.$n净产生的中子($\left.\begin{array}{l}{1}\\{0}\end{array}\right.$n)数为10NA |
15.人类对原子结构的认识经历了一个不断深入的过程,以下科学家中的哪位提出了原子结构中含有电子的学说( )
| A. | 汤姆生 | B. | 卢瑟福 | C. | 玻尔 | D. | 道尔顿 |
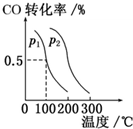 联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.