题目内容
14.下列叙述与盐类无关的是( )| A. | Na2CO3溶液不能盛装在玻璃塞的试剂瓶中 | |
| B. | 饱和食盐水使甲基橙显黄色 | |
| C. | FeCl3溶液加热蒸干得到Fe2O3 | |
| D. | 0.1mol/LCuCl2溶液中,c(Cu2+)<0.1mol/L |
分析 A、纯碱为强碱弱酸盐;
B、能使甲基橙使甲基橙变黄色黄色的可能为酸性、中性或碱性溶液;
C、氯化铁水解生成氢氧化铁和氯化氢,FeCl3溶液加热蒸干,氯化氢挥发,水解平衡正向进行,得到氢氧化铁灼烧得到氧化铁;
D、CuCl2属于强酸弱碱盐,能水解.
解答 解:A、Na2CO3水解显碱性,与二氧化硅反应硅酸钠和水,所以Na2CO3不能盛放在玻璃瓶中,故A正确;
B、甲基橙的显色范围pH为3.1-4.4,pH4.4的为黄色酸性溶液,pH>4.4的为碱性溶液,所以,能使甲基橙使甲基橙变黄色黄色的可能为酸性、中性或碱性溶液,饱和食盐水显示中性,和水解无关,故B错误;
C、氯化铁水解生成氢氧化铁和氯化氢,FeCl3溶液加热蒸干,氯化氢挥发,水解平衡正向进行,得到氢氧化铁灼烧得到氧化铁,与水解有关,故C正确;
D、CuCl2属于强酸弱碱盐,水解生成氢氧化铜,使铜离子浓度减小,故D正确.
故选:B.
点评 本题主要考查了盐类水解知识,侧重于基础知识的考查,题目难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
2.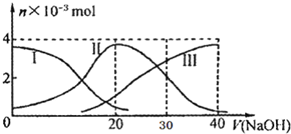 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-),根据图示判断,下列说法不正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-),根据图示判断,下列说法不正确的是( )
 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-),根据图示判断,下列说法不正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-),根据图示判断,下列说法不正确的是( )| A. | H2A在水中的电离方程式是:H2A═H++HA-;HA-═H++A2- | |
| B. | 当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| C. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水小 | |
| D. | 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2 c(OH-) |
9.下列装置或操作能达到相应实验目的是( )
| A. | 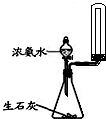 制备少量氨气 | B. | 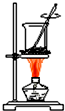 海带灼烧成灰 | ||
| C. | 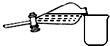 分液时取出下层液体 | D. | 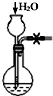 检查气密性 |
19. (1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度.则100℃时1mol•L-1的NaOH溶液中,由水电离出的c(H+)=1×10-12mol•L-1.25℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是促进(填“促进”、“抑制”或“不影响”).
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度.则100℃时1mol•L-1的NaOH溶液中,由水电离出的c(H+)=1×10-12mol•L-1.25℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是促进(填“促进”、“抑制”或“不影响”).
(2)电离平衡常数是衡量弱电解质电离程度强弱的量.已知如表数据.
①25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液显碱性,则c(Na+)>
c(CH3COO-)(填“>”、“<”或“=”).
②25℃时,有等浓度的①NaCN溶液、②Na2CO3溶液、③CH3COONa溶液,三种溶液的pH由大到小的顺序为Na2CO3溶液>NaCN溶液>CH3COONa溶液.(填序号)
③向NaCN溶液中通入少量CO2,所发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
 (1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度.则100℃时1mol•L-1的NaOH溶液中,由水电离出的c(H+)=1×10-12mol•L-1.25℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是促进(填“促进”、“抑制”或“不影响”).
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度.则100℃时1mol•L-1的NaOH溶液中,由水电离出的c(H+)=1×10-12mol•L-1.25℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是促进(填“促进”、“抑制”或“不影响”).(2)电离平衡常数是衡量弱电解质电离程度强弱的量.已知如表数据.
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
c(CH3COO-)(填“>”、“<”或“=”).
②25℃时,有等浓度的①NaCN溶液、②Na2CO3溶液、③CH3COONa溶液,三种溶液的pH由大到小的顺序为Na2CO3溶液>NaCN溶液>CH3COONa溶液.(填序号)
③向NaCN溶液中通入少量CO2,所发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
6.下列关于电解质溶液的叙述正确的是( )
| A. | 常温下,在NH4Cl溶液中离子浓度大小顺序为c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH小 |
3.下列晶体中,可能具有层状晶体的是( )
| A. | CaF2 | B. | Na2O | C. | CuSO4•5H2O | D. | FeCl3 |
4.下列物质久置于敞口容器中,不易变质的是( )
| A. | 次氯酸 | B. | 金属钠 | C. | 氯化钠 | D. | 氧化钙 |
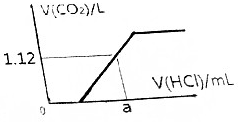 取Na2CO3和NaHCO3的混合物8.22g,加热到质量不再发生变化,冷却后称其质量为6.36g.
取Na2CO3和NaHCO3的混合物8.22g,加热到质量不再发生变化,冷却后称其质量为6.36g.