题目内容
6.下列关于电解质溶液的叙述正确的是( )| A. | 常温下,在NH4Cl溶液中离子浓度大小顺序为c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH小 |
分析 A.铵根离子水解,使溶液呈酸性,则c(H+)>c(OH-),一般情况下盐的水解程度都比较小,据此判断离子浓度大小;
B.稀释醋酸后,溶液中氢离子浓度减小,由于水的离子积不变,则氢氧根离子浓度增大;
C.醋酸为弱酸,pH相同时醋酸的浓度大于盐酸,则等体积时醋酸消耗的氢氧化钠的物质的量较大;
D.常温下,硫离子的第一步水解程度大于第二步,酸性越强,对应的酸根离子的水解程度越弱.
解答 解:A.铵根离子水解,使溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒可知c(Cl-)>c(NH4+),一般情况下盐的水解程度都比较小,所以溶液中离子浓度大小顺序为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),故A正确;
B.将pH=4的醋酸溶液稀释后,醋酸的电离程度增大,但是溶液中氢离子、醋酸根离子和醋酸的浓度都减小,由于水的离子积不变,溶液中氢氧根离子浓度会增大,故B错误;
C.中和pH与体积均相同的盐酸和醋酸溶液,醋酸为弱酸,则醋酸的浓度大于盐酸,所以醋酸消耗NaOH的物质的量大于盐酸,故C错误;
D.常温下,硫离子的第一步水解程度大于第二步,则H2S的酸性较强,所以同浓度的Na2S与NaHS溶液相比,Na2S的水解程度较大,其溶液的pH较大,故D错误;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,涉及盐的水解原理、弱电解质的电离平衡、离子浓度大小比较等知识,明确影响盐的水解原理、弱电解质的电离平衡为解答关键,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
10.在强酸性溶液中,可以大量共存的离子组是( )
| A. | Na+、K+、S2-、Cl- | B. | Al3+、Mg2+、SO42-、Cl- | ||
| C. | K+、Na+、SiO32-、NO3- | D. | K+、Na+、SO42-、CO32- |
14.下列叙述与盐类无关的是( )
| A. | Na2CO3溶液不能盛装在玻璃塞的试剂瓶中 | |
| B. | 饱和食盐水使甲基橙显黄色 | |
| C. | FeCl3溶液加热蒸干得到Fe2O3 | |
| D. | 0.1mol/LCuCl2溶液中,c(Cu2+)<0.1mol/L |
15.下列各组元素中,属于同一周期的是( )
| A. | H、Na | B. | Al、P | C. | O、Cl | D. | Mg、F |
16.除去下列物质中的杂质(括号中为杂质),选用试剂正确的是( )
| A. | Fe2O3(Al2O3)用盐酸 | B. | Cl2(HCl)用NaOH溶液 | ||
| C. | Mg(Al)用纯碱溶液 | D. | SO2(HCl)用饱和的NaHSO3溶液 |
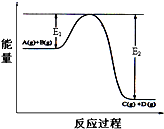 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.