题目内容
3.下列叙述中正确的是( )| A. | 金属原子失电子越多,其还原性越强 | |
| B. | 制成0.5L 1mol/L的Na2CO3溶液,需要Na2CO3•10H2O晶体质量为143克 | |
| C. | 相同条件下,NA个氧气分子和NA个氮气分子的密度比等于7:8 | |
| D. | 配制480 mL溶液时,选择规格为480 mL的容量瓶 |
分析 A、还原性与失电子的多少无关,与失电子的难易程度有关;
B、制成0.5L 1mol/L的Na2CO3溶液,需要Na2CO3•10H2O的物质的量为0.5mol,所以质量为:0.5mol×286g/mol=143g;
C、根据阿伏加德罗定律,物质的相同的气体的密度之比等于摩尔质量之比;
D、配制480 mL溶液时,选择规格为500 mL的容量.
解答 解:A、还原性与失电子的多少无关,与失电子的难易程度有关,越易失电子还原性越强,故A错误;
B、制成0.5L 1mol/L的Na2CO3溶液,需要Na2CO3•10H2O的物质的量为0.5mol,所以质量为:0.5mol×286g/mol=143g,故B正确;
C、根据阿伏加德罗定律,物质的相同的气体的密度之比等于摩尔质量之比,所以相同条件下,NA个氧气分子和NA个氮气分子的密度比等于8:7,故C错误;
D、配制480 mL溶液时,选择规格为500 mL的容量,故D错误;
故选B.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理是解题关键,注意容量瓶规格的选择方法,题目难度不大.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
14.下列不属于同分异构体的组合是:( )
| A. | 戊烷与乙烷 | B. | 淀粉和纤维素 | C. | 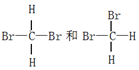 | D. | CH3CH2CH2CH3和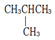 |
18.请根据你所学过的化学知识,判断下列说法中错误的是( )
| A. | 在使用加酶洗衣粉时先用开水冲泡洗衣粉,这样洗涤效果会增强 | |
| B. | 烧煤时可以加入少量石灰石,防止环境污染 | |
| C. | 氯化钠是家庭常用防腐剂,可用来腌制食品 | |
| D. | 家用水壶积存的水垢的主要成分是Mg(OH)2、CaCO3 |
8.下列反应的离子方程式,书写错误的是( )
| A. | 氢氧化钡跟硫酸铜溶液的反应:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓ | |
| B. | 石灰石溶于稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 少量的氢氧化钡与硫酸氢钠溶液混合:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 氯化铜溶液与铁粉反应:Cu2++Fe═Fe2++Cu |
10.在一定温度下,当Mg(OH)2固体在水溶液中达到下列平衡时:Mg(OH)2?Mg2++2OH-,要使Mg(OH)2固体减少而c(Mg2+)不变,可采取的措施是( )
| A. | 加MgSO4 | B. | 加HCl溶液 | C. | 加NaOH | D. | 加少量水 |
11.下列化学反应的离子方程式书写正确的是( )
| A. | 把金属铁放入稀硫酸中:Fe+2H+═Fe3++H2↑ | |
| B. | 往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 氢氧化铜加到盐酸中:Cu(OH)2+2H+═Cu2++2H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═Ba SO4↓+H2O |