题目内容
15.1L烷烃A的蒸汽完全燃烧时,生成同温同压下15L水蒸气,则该烷烃的分子式为( )| A. | C14H30 | B. | C15H32 | C. | C16H34 | D. | C17H36 |
分析 体积之比等于物质的量之比,根据H原子守恒计算烷烃A分子中H原子数目,结合烷烃的组成通式确定碳原子数目.
解答 解:1L烷烃A的蒸汽完全燃烧时,生成同温同压下15L水蒸气,则烷烃与水的物质的量之比为1:15,
根据H原子守恒,可知A分子中H原子数目为15×2=30,
烷烃的组成通式为CnH2n+2,则2n+2=30,解得n=14,故烷烃A的分子式为C14H30,
故选:A.
点评 本题考查有机物分子式的确定,注意原子守恒与组成通式的运用,有利于基础知识的巩固.

练习册系列答案
相关题目
5.下列说法正确的是(NA为阿伏加德罗常数)( )
| A. | 标准状况下,22.4 L苯所含分子数为NA | |
| B. | 1mol甲基所含电子数为10NA | |
| C. | 常温常压下,5.6 g乙烯与丁烯的混合物中含有的氢原子数目为0.8NA | |
| D. | 12 g金刚石中含有C-C键的个数为4NA |
10.根据原子结构及元素周期律的知识,下列推断正确的是( )
| A. | 1735Cl与1737Cl得电子能力相同 | |
| B. | 核外电子排布相同的微粒化学性质也相同 | |
| C. | Cl-、S2-、Ca2+、K+半径逐渐减小 | |
| D. | 同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
20.化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )

| A. | 该反应是吸热反应 | |
| B. | 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量 | |
| C. | 断裂1 mol A-A键和1 mol B-B键能放出x kJ能量 | |
| D. | 断裂2 mol A-B键需要吸收y kJ的能量 |
4.下列图示与对应的叙述相符的是( )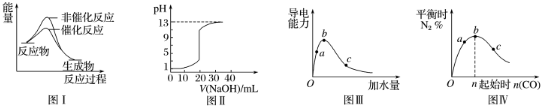

| A. | 图Ⅰ表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| B. | 图Ⅱ表示常温下,0.100 mol•L-1 NaOH溶液滴定20.00 mL 0.100 mol•L-1 HCl溶液所得到的滴定曲线 | |
| C. | 图Ⅲ表示一定质量的冰醋酸加水稀释过程中,醋酸溶液电离程度:c<a<b | |
| D. | 图Ⅳ表示反应4CO(g)+2NO2(g)?N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2转化率c>b>a |
5.工业上可通过CO和H2化合制得CH3OH:CO(g)+2H2(g)?CH3OH(g)△H(CO结构式为C≡O).又知某些化学键的键能(断开 1mol化学键时所需要的最低能量)数值如表:
则△H=-116 kJ•mol-1,在相应的反应条件下,将1mol CO(g)与足量H2混合充分反应后,放出或吸收的热量与△H的数值相对大小关系是<.
| 化学键 | C-C | C-H | H-H | C-O | C≡0 | H-O |
| 键能(kJ•mol-1) | 348.0 | 413.0 | 436.0 | 358.0 | 1072.0 | 463.0 |

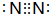 ;并写出由b生成c的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O
;并写出由b生成c的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O .
.