题目内容
20.化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )
| A. | 该反应是吸热反应 | |
| B. | 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量 | |
| C. | 断裂1 mol A-A键和1 mol B-B键能放出x kJ能量 | |
| D. | 断裂2 mol A-B键需要吸收y kJ的能量 |
分析 A.根据反应物的能量高于生成物的能量时,反应是放热反应;
B.根据图象可判断反应物与生成物的总能量;
C.根据旧键的断裂吸收能量,新键的生成释放能量分析;
D.根据旧键的断裂吸收能量.
解答 解:A.因反应物的能量高于生成物的能量时,反应是放热反应,故A错误;
B.由图可知,1molA2和1molB2的总能量高于2molAB的总能量,故B错误;
C.因旧键的断裂吸收能量,而不是释放能量,故C错误;
D.因旧键的断裂吸收能量,由图可知断裂2molA-B键需要吸收ykJ能量,故D正确;
故选D.
点评 本题考查学生有关化学反应中的能量变化知识,可以根据所学知识来进行,难度不大.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
10.食品保鲜膜的材质有聚乙烯(PE)、聚氯乙烯(PVC)等种类.下列叙述错误的是( )
| A. | 等质量的聚乙烯(PE)和乙烯完全燃烧消耗氧气的量相等 | |
| B. | 废弃的PE和PVC均可回收利用以减少白色污染 | |
| C. | 将PVC薄膜放入试管中加强热,产生的气体可使湿润的蓝色石蕊试纸变红 | |
| D. | PVC的单体可由PE的单体与氯化氢加成制得 |
15.1L烷烃A的蒸汽完全燃烧时,生成同温同压下15L水蒸气,则该烷烃的分子式为( )
| A. | C14H30 | B. | C15H32 | C. | C16H34 | D. | C17H36 |
12.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将0.1mol•L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液 | 先有白色沉淀生成后变为蓝色沉淀 | Cu(OH)2的Ksp比Mg(OH)2的小 |
| B | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+,无K+ |
| C | 向盛Na2SiO3 溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2min后,试管里出现凝胶 | 非金属性:Cl>Si |
| D | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状碳 | 浓硫酸具有吸水性和强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
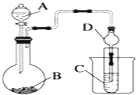
10.下列装置能达到实验目的是( )
| A. | 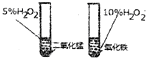 比较二氧化锰和氧化镁的催化效果 | B. | 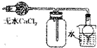 干燥收集氯气 | ||
| C. | 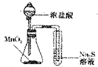 比较二氧化锰、氯气、硫的氧化性 | D. |  观察铁的吸氧腐蚀 |
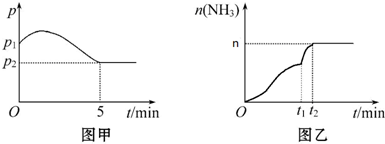
 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.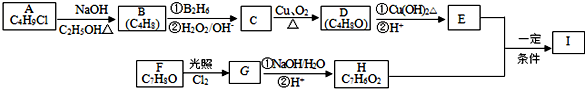
 ;
; ;
; .
.