题目内容
在一定温度下,向AgI的饱和溶液中:(填“增大”、“减小”或“不变”)
(1)若加入AgNO3固体,c(Ag+) ,c(I-) .
(2)若加入更多的AgI固体,则c(I-) .
(3)若加入AgBr固体,c(I-) .
(4)若加入Na2S固体,c(Ag+) ,c(I-) .
(1)若加入AgNO3固体,c(Ag+)
(2)若加入更多的AgI固体,则c(I-)
(3)若加入AgBr固体,c(I-)
(4)若加入Na2S固体,c(Ag+)
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:在一定温度下,向AgI的饱和溶液中存在沉淀溶解平衡,平衡状态下存在溶度积常数,依据平衡影响因素分析平衡的变化;
解答:
解:在一定温度下,向AgI的饱和溶液中存在沉淀溶解平衡,AgI(s)?Ag+(aq)+I-(aq),平衡状态下存在溶度积常数,Ksp=C(Ag+)?C(I-);
(1)若加入AgNO3固体,会增加银离子浓度,沉淀溶解平衡AgI(s)?Ag+(aq)+I-(aq),左移,c(I-)减小,故答案为:增大;减小;
(2)若加入更多的AgI固体,沉淀溶解平衡AgI(s)?Ag+(aq)+I-(aq),不变,则c(I-)不变,故答案为:不变;
(3)若加入固体AgBr,AgBr的溶解性大于AgI,所以平衡状态下AgBr溶液中的银离子浓度大于AgI溶液中的银离子浓度,所以碘化银沉淀溶解平衡左移,c(I-)减小,故答案为:减小;
(4)若加入Na2S固体,Ag2S的溶解性小于AgI,所以碘化银沉淀溶解平衡右移生成Ag2S沉淀,所以c(Ag+)减小,c(I-)增大,故答案为:减小;增大;
(1)若加入AgNO3固体,会增加银离子浓度,沉淀溶解平衡AgI(s)?Ag+(aq)+I-(aq),左移,c(I-)减小,故答案为:增大;减小;
(2)若加入更多的AgI固体,沉淀溶解平衡AgI(s)?Ag+(aq)+I-(aq),不变,则c(I-)不变,故答案为:不变;
(3)若加入固体AgBr,AgBr的溶解性大于AgI,所以平衡状态下AgBr溶液中的银离子浓度大于AgI溶液中的银离子浓度,所以碘化银沉淀溶解平衡左移,c(I-)减小,故答案为:减小;
(4)若加入Na2S固体,Ag2S的溶解性小于AgI,所以碘化银沉淀溶解平衡右移生成Ag2S沉淀,所以c(Ag+)减小,c(I-)增大,故答案为:减小;增大;
点评:本题考查了沉淀溶解平衡的分析判断和应用,主要是分析沉淀溶解平衡的影响因素的分析判断平衡移动的方向,题目较简单.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
下列物质的水溶液能导电,但属于非电解质的是( )
| A、HCl |
| B、Cl2 |
| C、NaHCO3 |
| D、CO2 |
在一定温度下难溶盐AgCl的饱和溶液中,Ag+与Cl-的物质的量浓度类似于水中c(H+)和c(OH-)的关系,即c(Ag+)c(Cl-)=Ksp(常数).在下列溶液中:
①30mL 0.02mol?L-1CaCl2溶液,②40mL 0.03mol?L-1盐酸,③10mLH2O,④50mL0.05mol?L-1AgNO3溶液,则AgCl的溶解度由大到小的顺序为( )
①30mL 0.02mol?L-1CaCl2溶液,②40mL 0.03mol?L-1盐酸,③10mLH2O,④50mL0.05mol?L-1AgNO3溶液,则AgCl的溶解度由大到小的顺序为( )
| A、①②③④ | B、③②①④ |
| C、④③①② | D、③②④① |
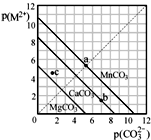 一定温度下,三种碳酸盐MCO3(M2+:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知 p(M2+)=-lgc(M2+),p(CO32-)=-lgc(CO32-).下列说法正确的是( )
一定温度下,三种碳酸盐MCO3(M2+:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知 p(M2+)=-lgc(M2+),p(CO32-)=-lgc(CO32-).下列说法正确的是( )| A、MgCO3、CaCO3、MnCO3的Ksp依次增大 |
| B、c点若表示MgCO3则为不饱和溶液,若表示CaCO3则有沉淀析出 |
| C、b点可表示CaCO3的饱和溶液,且Ca2+浓度与CO32-浓度相等 |
| D、在100mL MgCO3、CaCO3、MnCO3饱和的混和溶液中加入足量浓K2CO3溶液,产生沉淀MnCO3质量最多 |
已知某温度下,Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12,下列叙述正确的是( )
| A、向Ag2CrO4的浊液中加入AgNO3溶液,Ag2CrO4的Ksp减小 |
| B、将0.001 mol?L-1的AgNO3溶液逐滴加入到含Cl-和CrO42-浓度均为0.001 mol?L-1的溶液中,则先产生AgCl沉淀 |
| C、饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大 |
| D、该温度下,AgCl在水中的溶解度小于在食盐水中的溶解度 |