题目内容
复分解反应是中学化学中常见的一种反应类型.
(1)已知在常温下测得浓度均为0.1mol?L-1的下列6种溶液的pH值:
复分解存在这样一个规律:一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O 若换个角度看,它同时揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质.依照该规律,请判断下列反应不能成立的是 (填编号).
A.CO2+H2O+2NaClO═Na2CO3+2HClO
B.CO2+H2O+NaClO═NaHCO3+HClO
C.CO2+H2O+C6H5ONa→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH→NaHCO3+C6H5ONa
F.CH3COOH+NaCN═CH3COONa+HCN
(2)根据前述信息判断,常温下,浓度均为0.05mol?L-1的下列5种物质的溶液中,pH最小的是 (填编号),其pH值为 (填数值);pH最大的是 (填编号).
①HCN ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
(3)一些复分解反应的发生还遵循其它的规律.下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性钠溶液
②侯氏制碱法中,向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打晶体,请根据上述反应,总结出复分解反应发生的另一规律: .
(4)根据(3)中结论,现将KI溶液和AgCl固体混合搅拌,则可能会观察到的现象是 ,反应的离子方程式为 .
(1)已知在常温下测得浓度均为0.1mol?L-1的下列6种溶液的pH值:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
A.CO2+H2O+2NaClO═Na2CO3+2HClO
B.CO2+H2O+NaClO═NaHCO3+HClO
C.CO2+H2O+C6H5ONa→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH→NaHCO3+C6H5ONa
F.CH3COOH+NaCN═CH3COONa+HCN
(2)根据前述信息判断,常温下,浓度均为0.05mol?L-1的下列5种物质的溶液中,pH最小的是
①HCN ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
(3)一些复分解反应的发生还遵循其它的规律.下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性钠溶液
②侯氏制碱法中,向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打晶体,请根据上述反应,总结出复分解反应发生的另一规律:
(4)根据(3)中结论,现将KI溶液和AgCl固体混合搅拌,则可能会观察到的现象是
考点:探究化学规律,盐类水解的应用
专题:盐类的水解专题
分析:(1)根据一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,即强酸制取弱酸分析;
(2)浓度均为0.05mol/L的六种物质的溶液,氢离子浓度越大pH越小,反之越大,强酸的电离程度大于弱酸的电离程度;
(3)根据反应有沉淀生成,结合物质的溶解度情况来分析;
(4)碘化银的溶解度小于氯化银,沉淀可以向着更难溶的方向转化.
(2)浓度均为0.05mol/L的六种物质的溶液,氢离子浓度越大pH越小,反之越大,强酸的电离程度大于弱酸的电离程度;
(3)根据反应有沉淀生成,结合物质的溶解度情况来分析;
(4)碘化银的溶解度小于氯化银,沉淀可以向着更难溶的方向转化.
解答:
解:相同浓度的钠盐溶液,酸根离子水解程度越大,则钠盐溶液的pH越大,酸的酸性越小,根据钠盐溶液的PH知,酸性强弱顺序是:CH3COOH>H2CO3>HClO>HCN>C6H5OH,根据强酸制取弱酸判断,
A.酸性H2CO3>HClO>HCO3-,所以二氧化碳和次氯酸钠溶液反应生成碳酸氢钠,故错误;
B.酸性H2CO3>HClO>HCO3-,所以CO2+H2O+NaClO=NaHCO3+HClO成立,故正确;
C.酸性H2CO3>C6H5OH>HCO3-,应生成NaHCO3,故正确;
D.酸性H2CO3>C6H5OH>HCO3-,应生成NaHCO3,故错误;
E、酸性H2CO3>C6H5OH>HCO3-,应生成NaHCO3,故正确;
F、CH3COOH酸性大于HCN,所以反应CH3COOH+NaCN=CH3COONa+HCN能发生,故正确;
故选AD;
(2)浓度均为0.05mol/L的①HCN②CH3COOH③HClO4④HClO⑤H2SO4中,只有硫酸是二元强酸,电离出的氢离子浓度最大,所以酸性最强,pH最小,浓度均为0.05mol?L-1的硫酸中,c(H+)=0.1mol/L,所以pH=1,根据表中pH数据,知道HCN的酸性最弱,电离程度最小,所以氢离子浓最小,即①pH最大,
故答案为:⑤;1;①;
(3)由题意可知,三个反应都有沉淀生成,根据所给反应,总结出复分解反应发生的另一规律为:反应能够由溶解度相对较大的物质向生成溶解度相对较小的物质的方向进行,故答案为:复分解反应能向着生成更难溶物质的方向进行;
(4)KI溶液与AgCl固体混合搅拌,白色固体变为黄色,即发生反应:I-+AgCl=AgI+Cl-,证明生成了碘化银,故答案为:白色固体变为黄色;I-+AgCl=AgI+Cl-.
A.酸性H2CO3>HClO>HCO3-,所以二氧化碳和次氯酸钠溶液反应生成碳酸氢钠,故错误;
B.酸性H2CO3>HClO>HCO3-,所以CO2+H2O+NaClO=NaHCO3+HClO成立,故正确;
C.酸性H2CO3>C6H5OH>HCO3-,应生成NaHCO3,故正确;
D.酸性H2CO3>C6H5OH>HCO3-,应生成NaHCO3,故错误;
E、酸性H2CO3>C6H5OH>HCO3-,应生成NaHCO3,故正确;
F、CH3COOH酸性大于HCN,所以反应CH3COOH+NaCN=CH3COONa+HCN能发生,故正确;
故选AD;
(2)浓度均为0.05mol/L的①HCN②CH3COOH③HClO4④HClO⑤H2SO4中,只有硫酸是二元强酸,电离出的氢离子浓度最大,所以酸性最强,pH最小,浓度均为0.05mol?L-1的硫酸中,c(H+)=0.1mol/L,所以pH=1,根据表中pH数据,知道HCN的酸性最弱,电离程度最小,所以氢离子浓最小,即①pH最大,
故答案为:⑤;1;①;
(3)由题意可知,三个反应都有沉淀生成,根据所给反应,总结出复分解反应发生的另一规律为:反应能够由溶解度相对较大的物质向生成溶解度相对较小的物质的方向进行,故答案为:复分解反应能向着生成更难溶物质的方向进行;
(4)KI溶液与AgCl固体混合搅拌,白色固体变为黄色,即发生反应:I-+AgCl=AgI+Cl-,证明生成了碘化银,故答案为:白色固体变为黄色;I-+AgCl=AgI+Cl-.
点评:本题考查了强酸制弱酸的反应规律、盐类水解的应用,解题的重点是了解溶液酸碱性与pH的关系,属于基础性知识考查题,本题难度不大.

练习册系列答案
相关题目
 某温度时,BaSO4在水中的沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO42-(aq)Ksp=c(Ba2+)?c(SO42-),沉淀溶解平衡曲线如图所示,下列说法正确的是( )
某温度时,BaSO4在水中的沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO42-(aq)Ksp=c(Ba2+)?c(SO42-),沉淀溶解平衡曲线如图所示,下列说法正确的是( )| A、b点时c(Ba2+)?c(SO42- )小于Ksp |
| B、a点对应的Ksp等于c点对应的Ksp |
| C、加水稀释可以使溶液由b点变到c点 |
| D、加入适量的Na2SO4不可能使溶液由a点变到c点 |
用如图装置来制取并收集气体,你认为能制得的气体是( )


| A、用KMnO4粉末制取O2 |
| B、用浓氨水和CaO制取NH3 |
| C、用Zn和稀硫酸制取H2 |
| D、用石灰石和稀盐酸制取CO2 |
核糖是合成核酸的重要原料,其结构简式为:CH2OH-CHOH-CHOH-CHOH-CHO,下列关于核糖的叙述中,正确的是( )
| A、与葡萄糖互为同分异构体 |
| B、可以与银氨溶液作用形成银镜 |
| C、与葡萄糖互为同系物 |
| D、可以使石蕊试液变红 |
 如图是一种试验某气体化学性质的实验装置,图中B为开关. 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )
如图是一种试验某气体化学性质的实验装置,图中B为开关. 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )| A、浓H2SO4 |
| B、饱和NaCl溶液 |
| C、浓NaOH溶液 |
| D、饱和Na2CO3 |
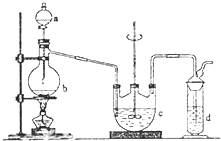 在实验室中可通过如下反应制取硫代硫酸钠Na2S2O3:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2
在实验室中可通过如下反应制取硫代硫酸钠Na2S2O3:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2