��Ŀ����
��һ���¶���������AgCl�ı�����Һ�У�Ag+��Cl-�����ʵ���Ũ��������ˮ��c��H+����c��OH-���Ĺ�ϵ����c��Ag+��c��Cl-��=Ksp������������������Һ�У�
��30mL 0.02mol?L-1CaCl2��Һ����40mL 0.03mol?L-1���ᣬ��10mLH2O����50mL0.05mol?L-1AgNO3��Һ����AgCl���ܽ���ɴ�С��˳��Ϊ��������
��30mL 0.02mol?L-1CaCl2��Һ����40mL 0.03mol?L-1���ᣬ��10mLH2O����50mL0.05mol?L-1AgNO3��Һ����AgCl���ܽ���ɴ�С��˳��Ϊ��������
| A���٢ڢۢ� | B���ۢڢ٢� |
| C���ܢۢ٢� | D���ۢڢܢ� |
���㣺���ܵ���ʵ��ܽ�ƽ�⼰����ת���ı���
ר�⣺����ƽ������Һ��pHר��
�����������Ȼ�����ˮ��Һ�д��ڳ����ܽ�ƽ�⣺AgCl��s��?Ag++Cl-����֪�����ӻ�������Ũ��Խ��ƽ�����ƣ��Ȼ������ܽ��ԽС��Ȼ����ѡ����������Ũ�ȴ�С�����Ȼ������ܽ�ȴ�С��
���
�⣺�����ӻ�������Ũ��Խ�Գ����ܽ�ƽ�����Ƴ̶�Խ���Ȼ����ܽ��ԽС��
��30ml 0.02mol/LCaCl2��Һ��������Ũ��Ϊ0.04 mol?L-1��
��40ml 0.03mol/LHCl��Һ��������Ũ��Ϊ0.03 mol?L-1��
��10ml����ˮ����ˮ�ٽ�AgCl��s��?Ag++Cl-�����ƶ���
��50ml 0.05mol/LAgNO3��Һ��������Ũ��Ϊ0.05 mol?L-1��
�������ϼ����֪��ѡ�٢ڢ������ܽ⣬���������Ũ��Խ�����Ƴ̶�Խ��AgCl�ڴ�������Һ�е��ܽ���ɴ�С��˳��Ϊ�ڢ٢ܣ������дٽ��ܽ⣬����C���Ȼ������ܽ�����˳��Ϊ���ۢڢ٢ܣ�
��ѡB��
��30ml 0.02mol/LCaCl2��Һ��������Ũ��Ϊ0.04 mol?L-1��
��40ml 0.03mol/LHCl��Һ��������Ũ��Ϊ0.03 mol?L-1��
��10ml����ˮ����ˮ�ٽ�AgCl��s��?Ag++Cl-�����ƶ���
��50ml 0.05mol/LAgNO3��Һ��������Ũ��Ϊ0.05 mol?L-1��
�������ϼ����֪��ѡ�٢ڢ������ܽ⣬���������Ũ��Խ�����Ƴ̶�Խ��AgCl�ڴ�������Һ�е��ܽ���ɴ�С��˳��Ϊ�ڢ٢ܣ������дٽ��ܽ⣬����C���Ȼ������ܽ�����˳��Ϊ���ۢڢ٢ܣ�
��ѡB��
���������⿼���˳����ܽ�ƽ���Ӱ�����ط����жϣ���Ŀ�ѶȲ�����Ҫ�������Ӵ�С���Ȼ����ܽ�ƽ���Ӱ���жϣ�������ض�ѧ������֪ʶ��ѵ���ͼ��飬���ѧ��������û���֪ʶ���ʵ�������������

��ϰ��ϵ�д�
�����Ŀ
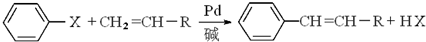 ��XΪ±ԭ�ӣ�RΪȡ������
��XΪ±ԭ�ӣ�RΪȡ������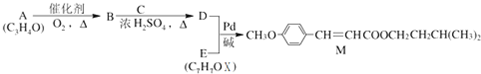
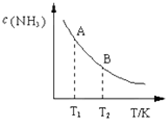 ���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ش��������⣺
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ش��������⣺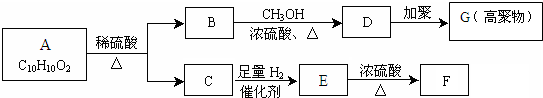
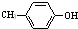 ��F��ʹ���CCl4��Һ��ɫ����ش��������⣺
��F��ʹ���CCl4��Һ��ɫ����ش��������⣺