题目内容
已知某温度下,Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12,下列叙述正确的是( )
| A、向Ag2CrO4的浊液中加入AgNO3溶液,Ag2CrO4的Ksp减小 |
| B、将0.001 mol?L-1的AgNO3溶液逐滴加入到含Cl-和CrO42-浓度均为0.001 mol?L-1的溶液中,则先产生AgCl沉淀 |
| C、饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大 |
| D、该温度下,AgCl在水中的溶解度小于在食盐水中的溶解度 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A、依据沉淀溶解平衡中的溶度积常数只随温度变化;
B、依据溶度积常数计算沉淀需要的银离子浓度大小比较分析;
C、由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=1.0×10-12,x3=2.0×10-12,即x═
,因为AgCl饱和溶液中Ag+的浓度为
,所以银离子浓度,Ag2CrO4>AgCl;
D、该温度下,AgCl在食盐水中的溶解度,氯离子存在沉淀溶解平衡逆向进行,氯化银溶解度减小,小于AgCl在水中的溶解度;
B、依据溶度积常数计算沉淀需要的银离子浓度大小比较分析;
C、由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=1.0×10-12,x3=2.0×10-12,即x═
| 3 | 2×10-12 |
| 1.56×10-10 |
D、该温度下,AgCl在食盐水中的溶解度,氯离子存在沉淀溶解平衡逆向进行,氯化银溶解度减小,小于AgCl在水中的溶解度;
解答:
解:A.KSP只于温度有关,与溶液中离子浓度无关.故A错误;
B.Ksp(AgCl)=c(Ag+)c(Cl-)=1.56×10-10,c(Ag+)=
=1.56×10-7mol/L,Ksp(Ag2CrO4)=c2(Ag+)c(CrO4 2-)=1×10-12,c(Ag+)=
=1×10-4.5mol/L,生成氯化银需要的银离子浓度小,所以先析出AgCl,故B正确;
C、由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=1.0×10-12,x3=2.0×10-12,即x═
,因为AgCl饱和溶液中Ag+的浓度为
,所以银离子浓度,Ag2CrO4>AgCl,饱和AgCl溶液与饱和Ag2CrO4溶液相比,后者的c(Ag+)大,故C错误;
D、该温度下,AgCl在食盐水中的溶解度,氯离子存在沉淀溶解平衡逆向进行,氯化银溶解度减小,小于AgCl在水中的溶解度,故D错误.
故选B.
B.Ksp(AgCl)=c(Ag+)c(Cl-)=1.56×10-10,c(Ag+)=
| 1.56×10-10 |
| 10-3 |
|
C、由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=1.0×10-12,x3=2.0×10-12,即x═
| 3 | 2×10-12 |
| 1.56×10-10 |
D、该温度下,AgCl在食盐水中的溶解度,氯离子存在沉淀溶解平衡逆向进行,氯化银溶解度减小,小于AgCl在水中的溶解度,故D错误.
故选B.
点评:本题考查了沉淀溶解平衡的理解应用,溶度积的计算分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
 某温度时,BaSO4在水中的沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO42-(aq)Ksp=c(Ba2+)?c(SO42-),沉淀溶解平衡曲线如图所示,下列说法正确的是( )
某温度时,BaSO4在水中的沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO42-(aq)Ksp=c(Ba2+)?c(SO42-),沉淀溶解平衡曲线如图所示,下列说法正确的是( )| A、b点时c(Ba2+)?c(SO42- )小于Ksp |
| B、a点对应的Ksp等于c点对应的Ksp |
| C、加水稀释可以使溶液由b点变到c点 |
| D、加入适量的Na2SO4不可能使溶液由a点变到c点 |
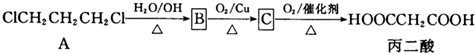
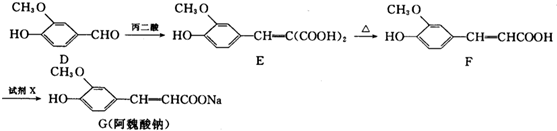

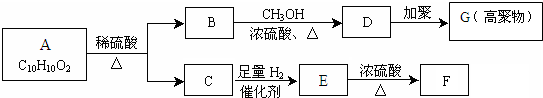
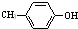 ,F能使溴的CCl4溶液褪色.请回答下列问题:
,F能使溴的CCl4溶液褪色.请回答下列问题: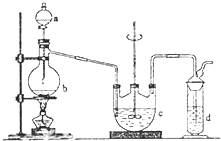 在实验室中可通过如下反应制取硫代硫酸钠Na2S2O3:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2
在实验室中可通过如下反应制取硫代硫酸钠Na2S2O3:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2