题目内容
20.0.5mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出1082.5kJ热量,其热化学反应方程式为:(B2H6)(g)+3O2(g)═B2O3(s)+3 H2O(l)△H=-2165kJ/mol;又知H2O(l)?H2O(g);△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是1016.5 kJ.分析 根据热化学方程式的书写方法可知,物质的物质的量与反应放出的热量成正比,并注意标明各物质的聚集状态来解答;写出热化学方程式,根据盖斯定律来分析.
解答 解:0.5mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出1082.5 kJ热量,则1mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出2×1082.5 kJ=2165KJ的热量,反应的热化学方程式为:B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2165 kJ•mol-1;
由于①B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2165kJ/mol,②H2O(l)→H2O(g);△H=+44kJ/moL,由盖斯定律可知①+②×3得:B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2033kJ/mol,11.2L(标准状况)即0.5mol乙硼烷完全燃烧生成气态水时放出的热量是2033kJ×0.5=1016.5kJ,
故答案为:B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2165kJ/mol;1016.5.
点评 本题考查了热化学方程式的书写方法和盖斯定律的计算应用以及热量的计算,需要注意的有:反应热的数值与化学方程式前面的系数成正比.题目难度中等.

练习册系列答案
相关题目
10.一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),进行反应,2SO2+O2?2SO3,其起始物质的量及SO2的平衡转化率如下表所示.下列判断中正确的是( )
| 甲 | 乙 | 丙 | 丁 | ||
| 密闭容器体积/L | 2 | 2 | 2 | 1 | |
| 起始物质的量 | n(SO2)/mol | 0.40 | 0.80 | 0.80 | 0.40 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2的平衡转化率% | 80 | α1 | α2 | α3 | |
| A. | 甲中反应的平衡常数小于乙 | |
| B. | 该温度下,该反应的平衡常数K为400 | |
| C. | SO2的平衡转化率:α1>α2=α3 | |
| D. | 容器中SO3的物质的量浓度:丙=丁<甲 |
5.(1)如图 I表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为5,量筒中液体的体积是3.6mL.
(2)如图 II表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)D.
A.是a mL B.是(50-a)mLC.一定大于a mL D.一定大于(50-a)mL
(3)某研究性学习小组为了探究醋酸的电离情况,进行了如实验.配制并标定醋酸溶液的浓度,取冰醋酸配制250mL 0.2mol•L-1的醋酸溶液,用0.2mol•L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定.回答下列问题:
①配制250mL 0.2mol•L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250 mL容量瓶.
②为标定某醋酸溶液的准确浓度,用0.200 0mol•L-1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如表:
则该醋酸溶液的准确浓度为0.2000 mol/L.(保留小数点后四位)
③关于该滴定实验,从下列选项中选出最恰当的一项D(选填字母).
探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸的pH,结果如表:
回答下列问题:
④根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:0.0100 mol•L-1醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于1.
⑤从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度将增大.(填“增大”“减小”或“不变”)
探究温度对醋酸电离程度的影响
⑥请你设计一个实验完成该探究,请简述你的实验方案:用pH计(或精密pH试纸)测定相同浓度的醋酸在几种不同温度时的pH.

(2)如图 II表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)D.
A.是a mL B.是(50-a)mLC.一定大于a mL D.一定大于(50-a)mL
(3)某研究性学习小组为了探究醋酸的电离情况,进行了如实验.配制并标定醋酸溶液的浓度,取冰醋酸配制250mL 0.2mol•L-1的醋酸溶液,用0.2mol•L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定.回答下列问题:
①配制250mL 0.2mol•L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250 mL容量瓶.
②为标定某醋酸溶液的准确浓度,用0.200 0mol•L-1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如表:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
③关于该滴定实验,从下列选项中选出最恰当的一项D(选填字母).
| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
用pH计测定25℃时不同浓度的醋酸的pH,结果如表:
| 醋酸浓度(mol•L-1) | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
④根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:0.0100 mol•L-1醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于1.
⑤从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度将增大.(填“增大”“减小”或“不变”)
探究温度对醋酸电离程度的影响
⑥请你设计一个实验完成该探究,请简述你的实验方案:用pH计(或精密pH试纸)测定相同浓度的醋酸在几种不同温度时的pH.
12.下列说法中正确的是( )
| A. | 过量的铜与浓硝酸反应有一氧化氮生成 | |
| B. | Al、Fe、Cu的单质放置在空气中均只生成氧化物 | |
| C. | SiO2与酸、碱均不反应 | |
| D. | 向一定浓度的Na2SiO3溶液中通入适量CO2气体,出现白色沉淀,则H2SiO3的酸性比H2CO3的酸性强 |
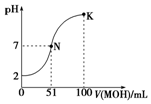 常温下,向100mL 0.01mol•L-1 HA溶液中逐滴加入0.02mol•L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
常温下,向100mL 0.01mol•L-1 HA溶液中逐滴加入0.02mol•L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题: 腐乳是桂林有名的特产之一,请参考图中的有关信息回答下列问题.
腐乳是桂林有名的特产之一,请参考图中的有关信息回答下列问题.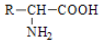 .腐乳虽好但不能作为主食,原因在于腐乳所含的糖类营养素较少,而该类营养素是人类生命活动所需能量的主要来源物质.
.腐乳虽好但不能作为主食,原因在于腐乳所含的糖类营养素较少,而该类营养素是人类生命活动所需能量的主要来源物质. .
.