题目内容
12.能正确表示下列反应的离子方程式的是( )| A. | 足量硫酸铝与纯碱反应:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ | |
| B. | 硫酸铜与烧碱反应:CuSO4+2OH-═Cu(OH)2↓+SO42- | |
| C. | 苯酚与碳酸钠反应:2C6H5OH+CO32-═2C6H5O-+CO2↑+H2O | |
| D. | 碳酸钡与硫酸反应:Ba2++SO42-═BaSO4↓ |
分析 A.铝离子与碳酸根离子发生双水解生成氢氧化铝和二氧化碳;
B.硫酸铜为可溶性盐,应拆成离子形式;
C.不符合反应客观事实;
D.碳酸钡为沉淀,应保留化学式.
解答 解:A.足量硫酸铝与纯碱反应生成氢氧化铝、二氧化碳和硫酸钠,离子方程式:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑,故A正确;
B.硫酸铜与烧碱反应,离子方程式:Cu2++2OH-═Cu(OH)2↓,故B错误;
C.苯酚与碳酸钠反应生成苯酚钠和碳酸氢钠,离子方程式:C6H5OH+CO32-═2C6H5O-+HCO3-,故C错误;
D.碳酸钡与硫酸反应,离子方程式:BaCO3+SO42═BaSO4↓+CO32-,故D错误;
故选:A.
点评 本题考查了离子方程式书写正误的判断,明确反应实质是解题关键,注意化学式拆分、注意离子反应遵循客观事实,题目难度不大.

练习册系列答案
相关题目
20.一定条件下,在密闭容器中进行如下反应:NO(g)+CO(g)?$\frac{1}{2}$N2(g)+CO2(g)△H=-373.2KJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| A. | 加催化剂同时升高温度 | B. | 加催化剂同时增大压强 | ||
| C. | 升高温度同时充入N2 | D. | 增大压强同时充入NO |
7.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1molBaCl2中含有的氯离子数为NA | |
| B. | 1mol镁原子中含有的电子数为2NA | |
| C. | 常温常压下,11.2LH2中含有的氢分子数为0.5NA | |
| D. | 16gO3中含有的氧原子数为NA |
17.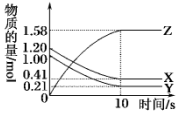 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应开始到10 s,用X表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应开始到10 s,Y的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应10s时达到化学平衡状态,Z的平衡浓度为0.79 mol•L-1 | |
| D. | 反应的化学方程式为2X(g)+2Y(g)?Z(g) |
4.下列说法正确的是( )
| A. | 高纯度的二氧化硅可用于制造计算机芯片和太阳能电池 | |
| B. | 胶体和溶液可以通过滤纸进行分离 | |
| C. | 雾是气溶胶,在阳光下可观察到丁达尔效应 | |
| D. | 玻璃是氧化物,成分可表示为Na2O•CaO•6SiO2 |
1.下列事实不能说明亚硝酸( HNO2)是弱电解质的是( )
| A. | HNO2不跟NaCl反应 | |
| B. | NaNO2溶液的pH大于7 | |
| C. | 常温下0.lmol/L HNO2溶液的pH为2.145 | |
| D. | 相同温度下,用相同浓度的HCl溶液和HNO2溶液作导电试验,HNO2溶液灯泡较暗 |