题目内容
17.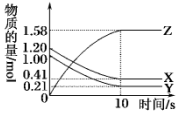 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应开始到10 s,用X表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应开始到10 s,Y的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应10s时达到化学平衡状态,Z的平衡浓度为0.79 mol•L-1 | |
| D. | 反应的化学方程式为2X(g)+2Y(g)?Z(g) |
分析 由图象可以看出,反应中x、Y的物质的量减少,应为反应物,z的物质的量增多,应为生成物,则有X:Y:Z=(1.20mol-0.41mol):(1.0mol-0.21mol):1.58mol=1:1:2,则反应的化学方程式为X+Y?2Z,以此解答该题.
解答 解:A.反应开始到10 s,用X表示的反应速率为$\frac{\frac{1.20mol-0.41mol}{2L}}{10s}$=0.0395mol•L-1•s-1,故A错误;
B.反应开始到10 s,Y的物质的量浓度减少了$\frac{1.0mol-0.21mol}{2L}$=0.395 mol•L-1,故B错误;
C.平衡时Z的物质的量为1.58mol,则Z的平衡浓度为0.79 mol•L-1,故C正确;
D.X:Y:Z=(1.20mol-0.41mol):(1.0mol-0.21mol):1.58mol=1:1:2,则反应的化学方程式为X+Y?2Z,故D错误.
故选C.
点评 本题考查物质的量随时间的变化曲线,以及化学平衡的计算,侧重于学生的分析能力和计算能力的考查,题目难度中等,注意把握化学方程式的判断方法.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
20.下列物质分类的正确组合是( )
| 选项 | 纯净物 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | 碱石灰 | 烧碱 | 氧化铝 | 二氧化碳 |
| B | NH3•H2O | 小苏打 | 氧化镁 | 二氧化氮 |
| C | 五水硫酸铜 | 纯碱 | 氧化钠 | 三氧化硫 |
| D | H2O2 | 苏打 | 过氧化钠 | 二氧化硫 |
| A. | A | B. | B | C. | C | D. | D |
8.设NA为阿伏加德罗常数,下列有关叙述正确的是( )
| A. | 1 molCu和足量的硫粉加热反应转移的电子数是2NA | |
| B. | 铜粉溶于1L0.5mol/L稀硝酸中,当生成标况下2.24LNO时,溶液中的氮原子数为0.4NA个 | |
| C. | 常温下,4.4克二氧化碳和二氧化氮中的混合物中氧原子数为0.2NA | |
| D. | 标准状况下,11.2升氯气溶于水,转移电子数为0.5 NA |
5.从下列提供的试剂和操作中选择最佳组合完成从碘水中提取单质碘( )
①酒精 ②苯 ③四氯化碳 ④分液 ⑤萃取 ⑥蒸馏.
①酒精 ②苯 ③四氯化碳 ④分液 ⑤萃取 ⑥蒸馏.
| A. | ②④ | B. | ②④⑤ | C. | ②④⑤⑥ | D. | ③④⑤⑥ |
12.能正确表示下列反应的离子方程式的是( )
| A. | 足量硫酸铝与纯碱反应:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ | |
| B. | 硫酸铜与烧碱反应:CuSO4+2OH-═Cu(OH)2↓+SO42- | |
| C. | 苯酚与碳酸钠反应:2C6H5OH+CO32-═2C6H5O-+CO2↑+H2O | |
| D. | 碳酸钡与硫酸反应:Ba2++SO42-═BaSO4↓ |
2.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 11.2 L CO2所含分子数为0.5 NA | |
| B. | 32gO2和O3的混合气体中含有的氧原子数为2NA | |
| C. | 标况下,11.2L乙醇(C2H5OH)中所含的碳原子数目为NA | |
| D. | 14.2 g Na2SO4固体中阴离子所带电荷数为0.1NA |
9.短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是其内层电子总数的3倍,Y原子最外层只有2个,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
| A. | 元素的简单气态氢化物的热稳定性X<W | |
| B. | 元素的最高价氧化物对应水化物的酸性:W<Z | |
| C. | 化合物YX、ZX2、WX3中化学键类型相同 | |
| D. | 原子半径的大小顺序:Y>Z>W>X |
6.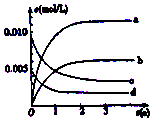 800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )
800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )
 800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )
800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO) (mol) | 0.020 | 0.010 | 0.009 | 0.008 | 0.008 | 0.008 |
| A. | a线表示NO2的变化趋势,则0~2s内v(NO2)=0.006mol/(L•s) | |
| B. | 800℃时,该反应的平衡常数K=1125L/mol | |
| C. | 能使该反应的反应速率增大,且平衡向正方向移动的措施是及时分理出NO2 | |
| D. | 已知:K300℃>K350℃,则该反应时吸热反应 |
7.某学习小组按如下实验过程(固定、加热及盛接仪器略)证明了海带中存在碘元素:
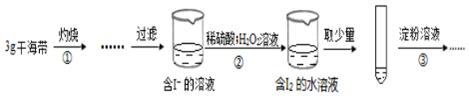
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 步骤①需要将干海带放入坩埚中灼烧 | |
| B. | 步骤②反应的离子方程式为:2I-+2H++H2O2=I2+2H2O | |
| C. | 步骤③操作后,观察到试管中溶液变为蓝色,可以说明海带中含有碘元素 | |
| D. | 若步骤②仅滴加稀硫酸后放置一会儿,步骤③操作后,试管中溶液颜色无明显变化 |