题目内容
1.下列事实不能说明亚硝酸( HNO2)是弱电解质的是( )| A. | HNO2不跟NaCl反应 | |
| B. | NaNO2溶液的pH大于7 | |
| C. | 常温下0.lmol/L HNO2溶液的pH为2.145 | |
| D. | 相同温度下,用相同浓度的HCl溶液和HNO2溶液作导电试验,HNO2溶液灯泡较暗 |
分析 能说明亚硝酸(HNO2)为弱电解质,可证明亚硝酸不能完全电离、存在电离平衡或对应的强碱盐溶液呈碱性,以此解答该题.
解答 解:A.HNO2不跟NaCl反应,不能说明亚硝酸是弱酸,故A选;
B.NaNO2溶液的pH大于7,说明发生水解,则亚硝酸钠是强碱弱酸盐,所以能说明亚硝酸是弱酸,故B不选;
C.0.lmol/L HNO2溶液的pH为2.145,说明亚硝酸不能完全电离,为弱电解质,故C不选;
D.用相同浓度的HCl溶液和HNO2溶液作导电试验,HNO2溶液灯泡较暗,则说明亚硝酸不能完全电离,能证明为弱电解质,故D不选;
故选A.
点评 本题考查弱电解质的实验设计的评价,侧重于考查学生实验评价能力和分析能力,注意把握弱电解质的电离特点和实验设计的角度,题目难度不大.

练习册系列答案
相关题目
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L空气中O2、N2分子总数目为NA | |
| B. | 0.1 mol羟基中所含电子数目为NA | |
| C. | 28 g乙烯、丙烯混合气体中所含原子数为6NA | |
| D. | 5.6 g铁与硝酸完全反应时转移的电子数目为0.3NA |
12.能正确表示下列反应的离子方程式的是( )
| A. | 足量硫酸铝与纯碱反应:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ | |
| B. | 硫酸铜与烧碱反应:CuSO4+2OH-═Cu(OH)2↓+SO42- | |
| C. | 苯酚与碳酸钠反应:2C6H5OH+CO32-═2C6H5O-+CO2↑+H2O | |
| D. | 碳酸钡与硫酸反应:Ba2++SO42-═BaSO4↓ |
9.短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是其内层电子总数的3倍,Y原子最外层只有2个,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
| A. | 元素的简单气态氢化物的热稳定性X<W | |
| B. | 元素的最高价氧化物对应水化物的酸性:W<Z | |
| C. | 化合物YX、ZX2、WX3中化学键类型相同 | |
| D. | 原子半径的大小顺序:Y>Z>W>X |
16.电解质是( )
| A. | 在水溶液里或溶融状态下全部电离的化合物 | |
| B. | 在水溶液里或熔融状态下能导电的化合物 | |
| C. | 可溶性盐类 | |
| D. | 导电性很强的物质 |
6.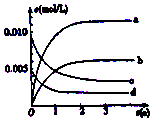 800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )
800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )
 800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )
800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO) (mol) | 0.020 | 0.010 | 0.009 | 0.008 | 0.008 | 0.008 |
| A. | a线表示NO2的变化趋势,则0~2s内v(NO2)=0.006mol/(L•s) | |
| B. | 800℃时,该反应的平衡常数K=1125L/mol | |
| C. | 能使该反应的反应速率增大,且平衡向正方向移动的措施是及时分理出NO2 | |
| D. | 已知:K300℃>K350℃,则该反应时吸热反应 |
13.已知Cr2O72-、Cr3+、CH3CH2OH、CH3COOH、H+、H2O六种微粒属于一个氧化还原反应中的反应物和生成物.下列叙述中不正确的是( )
| A. | 还原产物为CH3COOH | |
| B. | 氧化剂与还原剂的物质的量之比为2:3 | |
| C. | Cr2O72-和Cr3+分别属于反应物和生成物 | |
| D. | 若把该反应设计从成原电池,则负极反应为CH3CH2OH-4e-+H2O=CH3COOH+4H+ |
10.化学与生产、生活、社会、环境密切相关,下 列有关说法中错误的是( )
| A. | 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 | |
| B. | 石油裂解、煤的气化、葡萄糖制取酒精等过程中都包含化学变化 | |
| C. | 低碳经济就是以低能耗、低污染、低排放为基础的经济发展模式 | |
| D. | 食用植物油、麦芽糖和石油气都是纯净物 |
11.下列有关有机物的叙述中,正确的是( )
| A. | 淀粉与纤维素互为同分异构体 | |
| B. | 正丁烷的二氯代物有6种 | |
| C. | 糖类、油脂、蛋白质均为高分子化合物 | |
| D. | 乙烯使酸性高锰酸钾溶液褪色与乙烯使酸性重铬酸钾变色原理不同 |