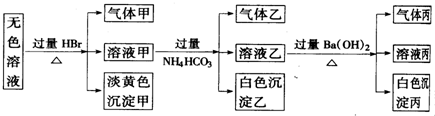
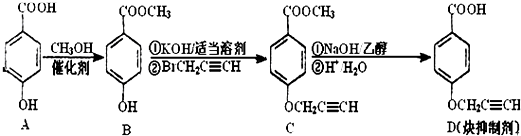
题目内容
下列有关实验装置正确的是( )
A、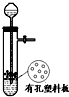 用于Cu和浓H2SO4反应制取少量的SO2气体 |
B、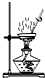 用于灼烧Al(OH)3 |
C、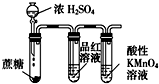 用于检验浓硫酸与蔗糖反应产生的二氧化硫 |
D、 由于实验室制备乙酸乙酯 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.Cu和浓H2SO4反应,需要加热;
B.灼烧Al(OH)3,应在坩埚中进行;
C.二氧化硫具有漂白性和还原性;
D.乙酸乙酯在NaOH溶液中水解.
B.灼烧Al(OH)3,应在坩埚中进行;
C.二氧化硫具有漂白性和还原性;
D.乙酸乙酯在NaOH溶液中水解.
解答:
解:A.Cu和浓H2SO4反应,需要加热,而图中缺少加热装置,故A错误;
B.灼烧Al(OH)3,应在坩埚中进行,不能在蒸发皿中灼烧,故B错误;
C.二氧化硫具有漂白性和还原性,则图中品红褪色,高锰酸钾褪色等可说明浓硫酸与蔗糖反应生成了二氧化硫,故C正确;
D.乙酸乙酯在NaOH溶液中水解,应将NaOH改为饱和碳酸钠溶液,故D错误;
故选C.
B.灼烧Al(OH)3,应在坩埚中进行,不能在蒸发皿中灼烧,故B错误;
C.二氧化硫具有漂白性和还原性,则图中品红褪色,高锰酸钾褪色等可说明浓硫酸与蔗糖反应生成了二氧化硫,故C正确;
D.乙酸乙酯在NaOH溶液中水解,应将NaOH改为饱和碳酸钠溶液,故D错误;
故选C.
点评:本题考查化学实验方案的评价,为高频考点,涉及常见物质的制备、氧化还原反应、性质实验及实验基本技能等,把握物质的性质、化学反应原理为解答的关键,侧重性质与原理的考查,注意实验的可行性、评价性分析,题目难度不大.

练习册系列答案
相关题目
已知25℃、101kPa下,碳、氢气、乙烯和葡萄糖的燃烧热依次是393.5kJ/mol、285.8kJ/mol、1411.0kJ/mol、2800kJ/mol,则下列热化学方程式正确的是( )
A、C(s)+
| ||
| B、2H2(g)+O2(g)═2H2O(g)△H=+571.6kJ/mol | ||
| C、C2H4(g)+3O2(g)═2CO2(g)+2H2O(g)△H=-1411.0kJ/mol-1 | ||
D、
|
pH=2的醋酸溶液1L,说法正确的是( )
| A、加入足量的Zn粒,产生标况下112mLH2 |
| B、加入NaOH固体后醋酸电离平衡右移,pH减小 |
| C、与一定量盐酸混合后pH=1,此时c(CH3COO-)+c(Cl-)+c(OH-)=0.1mol/L |
| D、加入冰醋酸,电离程度增大,pH减小 |
下列有关物质性质的应用错误的是( )
| A、二氧化硅不与强酸反应,可用石英玻璃容器盛放氢氟酸 |
| B、碳酸氢钠具有弱酸性,可用于食品发酵 |
| C、次氯酸钠具有强氧化性,可用于配制消毒液 |
| D、明矾能水解生成Al(OH)3胶体,可用作净水剂 |