题目内容
下列有关物质性质的应用错误的是( )
| A、二氧化硅不与强酸反应,可用石英玻璃容器盛放氢氟酸 |
| B、碳酸氢钠具有弱酸性,可用于食品发酵 |
| C、次氯酸钠具有强氧化性,可用于配制消毒液 |
| D、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
考点:硅和二氧化硅,氯、溴、碘及其化合物的综合应用,钠的重要化合物,镁、铝的重要化合物
专题:元素及其化合物
分析:A.二氧化硅常温下能够与氢氟酸反应;
B.碳酸氢钠性质不稳定受热易分解;
C.NaClO中Cl元素化合价为+1价,具有强氧化性;
D.明矾溶于水电离产生铝离子,铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性,能吸附水中的杂质;
B.碳酸氢钠性质不稳定受热易分解;
C.NaClO中Cl元素化合价为+1价,具有强氧化性;
D.明矾溶于水电离产生铝离子,铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性,能吸附水中的杂质;
解答:
解:A.玻璃的成分中含有二氧化硅,二氧化硅常温下能够与氢氟酸反应,能够腐蚀玻璃,不能用玻璃瓶盛放氢氟酸,故A错误;
B.碳酸氢钠受热易分解,可用于生产食品发酵粉,故B错误;
C.NaClO中Cl元素化合价为+1价,具有强氧化性,为84消毒液的有效成分,可用于杀菌消毒,故C正确;
D.明矾溶于水电离产生铝离子,铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性,能吸附水中的杂质,故可用作净水剂,故D正确;
故选:AB.
B.碳酸氢钠受热易分解,可用于生产食品发酵粉,故B错误;
C.NaClO中Cl元素化合价为+1价,具有强氧化性,为84消毒液的有效成分,可用于杀菌消毒,故C正确;
D.明矾溶于水电离产生铝离子,铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性,能吸附水中的杂质,故可用作净水剂,故D正确;
故选:AB.
点评:本题考查了元素化合物知识,熟悉碳酸盐、碳酸氢盐、次氯酸钠、二氧化硅、明矾的性质是解题关键,注意对基础知识的积累.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
下列有关实验装置正确的是( )
A、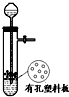 用于Cu和浓H2SO4反应制取少量的SO2气体 |
B、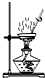 用于灼烧Al(OH)3 |
C、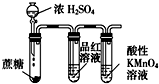 用于检验浓硫酸与蔗糖反应产生的二氧化硫 |
D、 由于实验室制备乙酸乙酯 |
下列叙述中,不正确的是( )
| A、玻璃、水泥、陶瓷都是硅酸盐产品 |
| B、水晶、玛瑙的主要成分都是SiO2 |
| C、硅元素在地壳中含量最多 |
| D、二氧化硅和大多数硅酸盐的化学性质都很稳定 |
常温下在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A、中性溶液:Cu2+、Al3+、NO3-、SO42- |
| B、加入苯酚显紫色的溶液:K+、NH4+、Cl-、NO3- |
| C、加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42- |
| D、常温下,c(H+)/c(OH-)=1×1012的溶液:K+、AlO2-、CO32-、Na+ |
尼泊金甲酯可在化妆品中作防腐剂,结构简式为: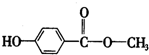 下列说法中正确的是( )
下列说法中正确的是( )
 下列说法中正确的是( )
下列说法中正确的是( )| A、在一定条件下,1 mol该物质最多能和2 mol NaOH反应 |
| B、该物质属于芳香烃 |
| C、该物质不能够和FeCl3反应 |
| D、该物质的分子式为C8H10O3 |