题目内容
某强酸性溶液X含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行实验,实验内容如下:
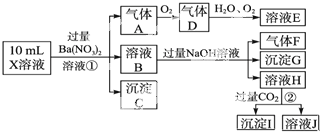
根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是 ;
(2)写出有关离子方程式:步骤①中生成A ;步骤②生成沉淀I .
(3)假设测定A、F、I 1mol,10mL X溶液中n(H+)=0.04mol,而沉淀C物质的量0.07mol,能说明该溶液不能确定的阴离子存在的理由是 .

根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是
(2)写出有关离子方程式:步骤①中生成A
(3)假设测定A、F、I
考点:常见阳离子的检验,常见阴离子的检验
专题:
分析:在强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有SO42-离子就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,以此解答.
解答:
解:在强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有SO42-离子就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,以此解答.
(1)在强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaOH和NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有SO42-离子就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,溶液X中除H+外还肯定含有的离子是Al3+、NH4+、Fe2+、SO42-;
故答案为:Al3+、NH4+、Fe2+、SO42-;
(2)①Fe2+离子被氧化为Fe3+离子,反应的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,步骤②生成沉淀I的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(3)A、F、I均为0.01mol,10mL X溶液中n(H+)=0.04mol,根据反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,可知Fe2+物质的量为0.03mol; 碳溶液中正电荷为:2n(Fe2+)+3n(Al3+)+n(NH4+)+n(H+)=2×0.03mol+3×0.01mol+0.01mol+0.04mol=0.14mol;沉淀C为硫酸钡,其物质的量0.07mol,n(SO42-)=0.07mol,硫酸根离子所带的负电荷为:0.07mol×2=0.14mol,说明溶液中正负电荷相等,所以若检验Fe3+肯定存在时,就有Cl-存在,因肯定存在的离子电荷总数已相等,
故答案为:若检验Fe3+肯定存在时,就有Cl-存在,因肯定存在的离子电荷总数已相等.
(1)在强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaOH和NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有SO42-离子就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,溶液X中除H+外还肯定含有的离子是Al3+、NH4+、Fe2+、SO42-;
故答案为:Al3+、NH4+、Fe2+、SO42-;
(2)①Fe2+离子被氧化为Fe3+离子,反应的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,步骤②生成沉淀I的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(3)A、F、I均为0.01mol,10mL X溶液中n(H+)=0.04mol,根据反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,可知Fe2+物质的量为0.03mol; 碳溶液中正电荷为:2n(Fe2+)+3n(Al3+)+n(NH4+)+n(H+)=2×0.03mol+3×0.01mol+0.01mol+0.04mol=0.14mol;沉淀C为硫酸钡,其物质的量0.07mol,n(SO42-)=0.07mol,硫酸根离子所带的负电荷为:0.07mol×2=0.14mol,说明溶液中正负电荷相等,所以若检验Fe3+肯定存在时,就有Cl-存在,因肯定存在的离子电荷总数已相等,
故答案为:若检验Fe3+肯定存在时,就有Cl-存在,因肯定存在的离子电荷总数已相等.
点评:本题考查物质的检验与鉴别,属于中等难度的试题,试题综合性强,难度较大,有利于培养学生的逻辑思维能力和发散思维能力,提高学生的应试能力和学习效率,要依据物质的特殊性质和特征反应来判断、推理、验证.

练习册系列答案
相关题目
向0.1mol/L的NaOH溶液慢慢滴加同浓度的醋酸溶液,离子浓度之间的关系不可能出现的是( )
| A、c(CH3COO-)>c(H+)>c(Na+ )>c(OH-) |
| B、c(Na+ )>c(OH-)>c(CH3COO-)>c(H+ ) |
| C、c(OH-)>c(Na+ )>c(H+ )>c(CH3COO-) |
| D、c(Na+ )>c(CH3COO-)>c(OH-)>c(H+ ) |
用铝箔包裹0.1mol金属钠,用针在铝箔上扎一些小孔,用镊子夹住,放入水中,待完全反应后,收集到的气体在标准状况下的体积为( )
| A、等于1.12L |
| B、等于0.56L |
| C、大于1.12L |
| D、小于1.12L |
将15g两种金属的混合物投入足量的盐酸中,反应完全后得到H2 11.2L(标准状况)该混合物的组成可能是( )
| A、钠和铁 | B、镁和铜 |
| C、铝和镁 | D、锌和铁 |
化学已渗透到人类生活的各个方面.下列说法不正确的是( )
| A、阿司匹林具有解热镇痛作用 |
| B、可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| C、红宝石、珍珠、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐 |
| D、石油裂解、煤的气化、海水制镁、纤维素制火棉等过程中都包含化学变化 |