题目内容
在一定温度下,将2mol A和2mol B两种气体混合于2L密闭容器中,发生反应3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成0.8molD,并测得C的浓度为0.4mol/L.由此推断:
(1)x值等于 .
(2)B的平衡浓度为 .
(3)A的转化率为 .
(4)生成D的反应速率 .
(5)如果增大反应体系的压强,则平衡体系中C的质量分数 .(填“增大”或“减小”或“不变”)
(1)x值等于
(2)B的平衡浓度为
(3)A的转化率为
(4)生成D的反应速率
(5)如果增大反应体系的压强,则平衡体系中C的质量分数
考点:化学平衡的计算,化学平衡的影响因素
专题:化学平衡专题
分析:2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol/L,物质的量=0.4mol/L×2L=0.8mol,反应之比等于化学方程式计量数之比,则x:2=0.8:0.8=1:1,则x=2,依据化学平衡三段式列式计算,
3A(g)+B(g)?2C(g)+2D(g)
起始量(mol) 2 2 0 0
变化量(mol) 1.2 0.4 0.8 0.8
平衡量(mol) 1.8 1.6 0.8 0.8
(1)依据反应比等于化学方程式计量数之比得到x;
(2)B浓度C=
;
(3)转化率=
×100%;
(4)反应速率v=
计算得到;
(5)增大压强,平衡不移动;
3A(g)+B(g)?2C(g)+2D(g)
起始量(mol) 2 2 0 0
变化量(mol) 1.2 0.4 0.8 0.8
平衡量(mol) 1.8 1.6 0.8 0.8
(1)依据反应比等于化学方程式计量数之比得到x;
(2)B浓度C=
| n |
| V |
(3)转化率=
| 消耗量 |
| 起始量 |
(4)反应速率v=
| △c |
| △t |
(5)增大压强,平衡不移动;
解答:
解:2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol/L,物质的量=0.4mol/L×2L=0.8mol,反应之比等于化学方程式计量数之比,则x:2=0.8:0.8=1:1,则x=2,依据化学平衡三段式列式计算,
3A(g)+B(g)?2C(g)+2D(g)
起始量(mol) 2 2 0 0
变化量(mol) 1.2 0.4 0.8 0.8
平衡量(mol) 1.8 1.6 0.8 0.8
(1)依据反应比等于化学方程式计量数之比得到x,分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol/L,物质的量=0.4mol/L×2L=0.8mol,反应之比等于化学方程式计量数之比,则x:2=0.8:0.8=1:1,则x=2,故答案为:2;
(2)B的平衡浓度c=
=
=0.8mol/L,;故答案为:0.8mol/L;
(3)A转化率=
×100%=
×100%=60%;
故答案为:60%;
(4)用D表示的平均反应速率v=
=
=0.2mol?l-1?min-1;
故答案为:0.2mol?l-1?min-1;
(5)3A(g)+B(g)?2C(g)+2D(g),反应是气体体积不变的反应,增大压强,平衡不移动,平衡体系中C的质量分数不变;
故答案为:不变;
3A(g)+B(g)?2C(g)+2D(g)
起始量(mol) 2 2 0 0
变化量(mol) 1.2 0.4 0.8 0.8
平衡量(mol) 1.8 1.6 0.8 0.8
(1)依据反应比等于化学方程式计量数之比得到x,分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol/L,物质的量=0.4mol/L×2L=0.8mol,反应之比等于化学方程式计量数之比,则x:2=0.8:0.8=1:1,则x=2,故答案为:2;
(2)B的平衡浓度c=
| n |
| V |
| 1.6mol |
| 2L |
(3)A转化率=
| 消耗量 |
| 起始量 |
| 1.2mol |
| 2mol |
故答案为:60%;
(4)用D表示的平均反应速率v=
| △c |
| △t |
| ||
| 2min |
故答案为:0.2mol?l-1?min-1;
(5)3A(g)+B(g)?2C(g)+2D(g),反应是气体体积不变的反应,增大压强,平衡不移动,平衡体系中C的质量分数不变;
故答案为:不变;
点评:本题考查了化学平衡计算应用,主要是反应物 抓化率,化学反应速率概念的计算应用,掌握基础是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
有机物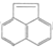 的一元取代物有( )
的一元取代物有( )
 的一元取代物有( )
的一元取代物有( )| A、3种 | B、4种 | C、6种 | D、8种 |
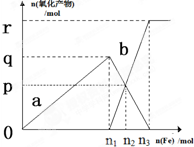 含有4.0mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示(还原产物只有NO).下列有关判断正确的是( )
含有4.0mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示(还原产物只有NO).下列有关判断正确的是( )| A、a是Fe(NO3)2 |
| B、n1=0.80 |
| C、p=0.60 |
| D、n3=1.20 |
制备普通玻璃的主要原料是( )
| A、Na2SiO3 |
| B、CaCO3 |
| C、Na2CO3 |
| D、SiO2 |