题目内容
用铝箔包裹0.1mol金属钠,用针在铝箔上扎一些小孔,用镊子夹住,放入水中,待完全反应后,收集到的气体在标准状况下的体积为( )
| A、等于1.12L |
| B、等于0.56L |
| C、大于1.12L |
| D、小于1.12L |
考点:化学方程式的有关计算,钠的化学性质,铝的化学性质
专题:
分析:Na和水反应生成NaOH和H2,NaOH和Al反应生成H2和NaAlO2,其方程式为Na+Al+2H2O=NaAlO2+2H2↑,根据Na和氢气之间的关系式计算.
解答:
解:Na和水反应生成NaOH和H2,NaOH和Al反应生成H2和NaAlO2,其方程式为Na+Al+2H2O=NaAlO2+2H2↑,根据方程式知,0.1molNa完全反应生成V(H2)=2n(Na).Vm=2×0.1mol×22.4L/mol=4.48L>1.12L,
故选C.
故选C.
点评:本题考查了物质间的反应,涉及钠和水的反应、铝和氢氧化钠溶液的反应,很多同学往往漏掉Al与NaOH溶液的反应而导致错误,为易错题.

练习册系列答案
相关题目
下列化合物的1H-NMR谱图中吸收峰数目正确的是( )
| A、CH3CH2CH2CH3(3个) |
B、 |
| C、CH2=CHCH2CH3(2个) |
D、 |
除去NaHCO3溶液中混有的少量Na2CO3可采取的方法是( )
| A、加入澄清石灰水 |
| B、加入氢氧化钡溶液 |
| C、通入二氧化碳气体 |
| D、加入稀盐酸 |
C、N、S都是重要的非金属元素,下列说法正确的是( )
| A、三者对应的氧化物均为酸性氧化物 |
| B、实验室可用NaOH溶液处理NO2和HCl废气 |
| C、三者的单质直接与氧气反应都能生成两种氧化物 |
| D、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
有机物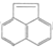 的一元取代物有( )
的一元取代物有( )
 的一元取代物有( )
的一元取代物有( )| A、3种 | B、4种 | C、6种 | D、8种 |
下列各组物质混合后,有气体生成,最终又有沉淀或固体析出的是( )
| A、过量氢氧化钠溶液和硫酸铝溶液 |
| B、氢氧化钠溶液和过量碳酸氢钠溶液 |
| C、少量铜粉和氯化铁溶液 |
| D、过氧化钠和少量氯化亚铁溶液 |