题目内容
硫酸是工业生产中最为重要的产品之一,也是化学工业的重要原料
(1)在硫酸工业生产中,我国采用黄铁矿为原料(与氧气反应)生产SO2,进料前必须将黄铁矿粉碎,目的是 .
(2)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据表信息,结合工业生产实际,选择最合适的生产条件是 .
(3)利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.
已知在T2温度时:2SO2(g)+O2(g)?2SO3(g);△H=-196.6kJ?mol-1,
①在T1温度时,该反应的平衡常数K=
,若在此温度下,向10L的恒容密闭容器中,充入0.3mol SO2(g)、1.6mol O2(g) 和0.3mol SO3(g),则反应开始时正反应速率 逆反应速率(填“<”、“>”或“=”).
②在T2温度时,开始在10L的密闭容器中加入4.0mol SO2(g)和10mol O2(g),一定条件下当反应达到平衡时共放出热量196.6kJ.此时二氧化硫的转化率为 .
③在②中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是 (填字母).
A.保持温度和容器体积不变,充入1mol O2(g)
B.保持温度和容器体积不变,充入2mol SO3 (g)
C.降低温度
D.在其他条件不变时,减小容器的容积.
(1)在硫酸工业生产中,我国采用黄铁矿为原料(与氧气反应)生产SO2,进料前必须将黄铁矿粉碎,目的是
(2)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据表信息,结合工业生产实际,选择最合适的生产条件是
| 压强 SO2转化率 温度 | 1个大气压 | 5个大气压 | 10个大气压 | 15个大气压 |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9988 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8520 | 0.8897 | 0.9276 | 0.9468 |
已知在T2温度时:2SO2(g)+O2(g)?2SO3(g);△H=-196.6kJ?mol-1,
①在T1温度时,该反应的平衡常数K=
| 10 |
| 3 |
②在T2温度时,开始在10L的密闭容器中加入4.0mol SO2(g)和10mol O2(g),一定条件下当反应达到平衡时共放出热量196.6kJ.此时二氧化硫的转化率为
③在②中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是
A.保持温度和容器体积不变,充入1mol O2(g)
B.保持温度和容器体积不变,充入2mol SO3 (g)
C.降低温度
D.在其他条件不变时,减小容器的容积.
考点:化学平衡的影响因素,浓度、温度、催化剂对化学反应速率的影响
专题:
分析:(1)将固体物质粉碎,可增大接触面积,加快反应速率,使黄铁矿反应更充分;
(2)根据SO2的转化率及生产成本来选择.
(3)①根据平衡常数和浓度商的大小综合判断;
②先根据平衡常数计算出c(SO2),再根据转化率公式求出SO2的转化率;
③根据浓度、温度、压强等外界条件对化学平衡的影响,求出平衡移动后c(SO2),
(2)根据SO2的转化率及生产成本来选择.
(3)①根据平衡常数和浓度商的大小综合判断;
②先根据平衡常数计算出c(SO2),再根据转化率公式求出SO2的转化率;
③根据浓度、温度、压强等外界条件对化学平衡的影响,求出平衡移动后c(SO2),
解答:
解:(1)将固体物质粉碎,可增大接触面积,加快反应速率,使黄铁矿反应更充分;故答案为:增大接触面积,加快反应速率,使黄铁矿反应更充分;
(2)因为SO2与O2的反应是放热反应,所以选择的温度为400℃,而1个标准大气压时SO2的转化率已经很大,再增大压强,SO2的转化率提高不大,但会增加生产成本,所以选择1个标准大气压,故答案为:400℃,1个标准大气压;
(3)①因为浓度商QC=
=6.2>K=
,所以化学反应逆向进行,即v(正)<v(逆),故答案为:<;
②在T2温度时,开始在10L的密闭容器中加入4.0molSO2和10.0molO2,一定条件下当反应达到平衡时共放出热量196.6kJ,根据1molSO2完全反应放热98.3KJ;则一定条件下当反应达到平衡时共放出热量196kJ,消耗二氧化硫物质的量=
=2mol;依据化学平衡三段式列式计算:
2 SO2(g)+O2(g)?2SO3(g)
开始量(mol) 4 10 0
变化量(mol) 2 1 2
平衡量(mol) 2 9 2
所以SO2的转化率α=
×100%=50%,故答案为:50%;
③A、保持温度和容器体积不变,O2的浓度增大,平衡正向移动,SO2的浓度减小,所以A正确;
B、保持温度和容器内压强不变,充入2mol SO3 (g)相当于充入2.0molSO2和5.0molO2,新的平衡与原平衡等效,SO2的浓度不变,所以B错误;
C、降低温度,平衡向放热的方向移动,而正反应为放热,所以平衡正向移动,SO2的浓度减小,所以C正确;
D、在其他条件不变时,减小容器的容积,SO2的浓度瞬间增大,之后平衡向气体体积减少的方向移动,即向正反应方向移动,SO2的浓度减小,再次到达平衡时SO2的浓度仍比原来大,所以D错误.
故答案为:AC;
(2)因为SO2与O2的反应是放热反应,所以选择的温度为400℃,而1个标准大气压时SO2的转化率已经很大,再增大压强,SO2的转化率提高不大,但会增加生产成本,所以选择1个标准大气压,故答案为:400℃,1个标准大气压;
(3)①因为浓度商QC=
| (0.03mol/L)2 |
| (0.03mol/L)2×0.16mol/L |
| 10 |
| 3 |
②在T2温度时,开始在10L的密闭容器中加入4.0molSO2和10.0molO2,一定条件下当反应达到平衡时共放出热量196.6kJ,根据1molSO2完全反应放热98.3KJ;则一定条件下当反应达到平衡时共放出热量196kJ,消耗二氧化硫物质的量=
| 1mol×196.6KJ |
| 98.3KJ |
2 SO2(g)+O2(g)?2SO3(g)
开始量(mol) 4 10 0
变化量(mol) 2 1 2
平衡量(mol) 2 9 2
所以SO2的转化率α=
| 2mol |
| 4mol |
③A、保持温度和容器体积不变,O2的浓度增大,平衡正向移动,SO2的浓度减小,所以A正确;
B、保持温度和容器内压强不变,充入2mol SO3 (g)相当于充入2.0molSO2和5.0molO2,新的平衡与原平衡等效,SO2的浓度不变,所以B错误;
C、降低温度,平衡向放热的方向移动,而正反应为放热,所以平衡正向移动,SO2的浓度减小,所以C正确;
D、在其他条件不变时,减小容器的容积,SO2的浓度瞬间增大,之后平衡向气体体积减少的方向移动,即向正反应方向移动,SO2的浓度减小,再次到达平衡时SO2的浓度仍比原来大,所以D错误.
故答案为:AC;
点评:本题考查了化学平衡的有关知识,如利用浓度商判断化学反应进行的方向,转化率的计算、外界条件对化学平衡的影响以及有关化学计算,沉淀转化的计算应用,试题较灵活,综合性强.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
请据图回答,经数小时后,U形管A、B两处的液面会出现下列哪种情况(实验装置足以维持过程中小白鼠的生命活动,瓶口密封,忽略水蒸汽和温度对实验结果的影响)

| A、A处上升,B处下降 |
| B、A、B两处都下降 |
| C、A处下降,B处上升 |
| D、A、B两处都不变 |
在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是( )
| A、氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 |
| B、向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
| C、向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO |
| D、向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- |
除去NaHCO3溶液中混有的少量Na2CO3可采取的方法是( )
| A、加入澄清石灰水 |
| B、加入氢氧化钡溶液 |
| C、通入二氧化碳气体 |
| D、加入稀盐酸 |
有机物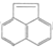 的一元取代物有( )
的一元取代物有( )
 的一元取代物有( )
的一元取代物有( )| A、3种 | B、4种 | C、6种 | D、8种 |
反应mA(g)+nB(g)?pC(g)中,若VA=a mol/(L?s),则VC为( )
A、
| ||
B、
| ||
C、
| ||
D、
|