题目内容
10.粗铜中含多种杂质(如锌、金和银等),工业上常用电解精炼法将粗铜提纯,在电解精炼时( )| A. | 精炼时粗铜接电源负极 | |
| B. | 精炼时纯铜作阴极 | |
| C. | 杂质都将以单质形式沉积到池底 | |
| D. | 纯铜片增重2.56 g,电路中通过电子为0.04 mol |
分析 A、电解精炼铜,粗铜作阳极,与电源正极相连;
B、电解精炼铜,粗铜作阳极,精铜作阴极;
C、不参与阳极放电的金属单质以及杂质会形成阳极泥;
D、精铜片增重2.56g,即析出2.56g铜,则电路中通过电子为$\frac{2.56}{64}$×2=0.08mol.
解答 解:A、电解精炼铜,粗铜作阳极,粗铜作阳极,与电源正极相连,故A错误;
B、电解精炼铜,粗铜作阳极,纯铜作阴极,故B正确;
C、在阳极上,不参与放电的金属单质金、银等贵重金属以及杂质会形成阳极泥沉积到池底,而比铜活泼的金属以离子进入溶液,故C错误;
D、精铜片增重2.56g,即析出2.56g铜,则电路中通过电子为$\frac{2.56}{64}$×2=0.08mol,故D错误;
故选B.
点评 本题考查学生电解精炼铜的原理,注意电解池的工作原理是关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.向FeCl3溶液中,加入下列哪种物质能使溶液变为血红色 ( )
| A. | NaOH溶液 | B. | 铁片 | C. | KSCN溶液 | D. | 石蕊溶液 |
18.化学与人类生成、生活密切相关,下列有关说法错误的为( )
| A. | 以淀粉为原料可以制取乙酸乙酯 | |
| B. | 福尔马林可用于浸制标本,是因为其能使蛋白质变性 | |
| C. | 医用酒精通常是指体积分数为75%的乙醇溶液 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
15.在蒸发皿中加热蒸干再加热(低于400℃)下列物质的溶液可以得到该物质固体的是( )
| A. | 氯化铝 | B. | 碳酸氢钠 | C. | 高锰酸钾 | D. | 硫酸钠 |
2.下列有关化学与生活、工业的叙述中,不正确的是( )
| A. | 工业生产玻璃、水泥、漂白粉及用铁矿石冶炼铁,均需要用石灰石为原料 | |
| B. | CO会与血红蛋白结合,使人中毒;可将中毒病人放入高压氧仓中解毒,其解毒原理符合平衡移动原理 | |
| C. | 2011年5月份起,面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物,过氧化苯甲酰属于有机物 | |
| D. | 固体煤经处理变为气体燃料后,可以减少SO2和烟尘的排放,且燃烧效率提高,有利于“节能减排” |
19.下列各组离子在溶液中能大量共存的是( )
| A. | 酸性溶液Na+、K+、MnO4-、Fe2+ | B. | 酸性溶液Fe3+、NH4+、SCN-、NH3+ | ||
| C. | 碱性溶液Na+、K+、AlO2-、SO42- | D. | 碱性溶液Ba2+、Na+、HCO3-、Cl- |
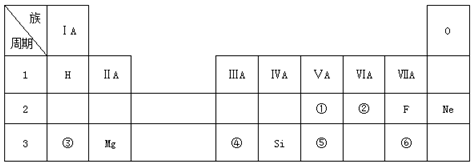
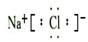 .
.