题目内容
20.在P+CuSO4+H2O-Cu3P+H3PO4+H2SO4 (未配平)反应中,下列说法正确的是( )| A. | CuSO4只做还原剂 | |
| B. | 10mol CuSO4可氧化P的物质的量为2mol | |
| C. | Cu3P既是氧化产物,又是还原产物 | |
| D. | 生成1mol Cu3P时,被氧化的P的物质的量为2.2mol |
分析 P+CuSO4+H2O-Cu3P+H3PO4+H2SO4 反应中P元素的化合价由0升高为+5价,P元素的化合价由0降低为-3价,则P既是氧化剂又是还原剂,生成Cu3P为还原产物,H3PO4为氧化产物,Cu元素的化合价由+2价降低为+1价,则CuSO4为氧化剂,生成Cu3P为还原产物,以此来解答.
解答 解:A.Cu元素的化合价由+2价降低为+1价,则CuSO4为氧化剂,故A错误;
B.Cu元素的化合价由+2价降低为+1价,P元素的化合价由0升高为+5价,由得失电子守恒,则10mol CuSO4可氧化P的物质的量为$\frac{10×(2-1)}{5-0}$moL=2mol,故B正确;
C.根据以上分析,Cu3P仅为还原产物,故C错误;
D.由电子守恒可知,生成1mol Cu3P时,被氧化的P的物质的量为$\frac{1×3+1×(3-1)}{5-0}$mol=1.2mol,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.

练习册系列答案
相关题目
8.高氯酸是一种酸性极强的无机含氧酸,可用于制备高氯酸盐、人造金刚石提纯等方面.
查阅资料得到以下有关高氯酸的信息:
工业上生产高氯酸的同时还生产了亚氯酸钠,工业流程如图:
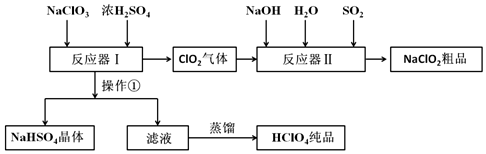
(1)操作①的名称是过滤.
(2))Ca(ClO)2、ClO2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有强氧化性
(3)反应器Ⅰ中投料时需加入过量浓硫酸,请简述目的为了产物能得到HClO4而不是NaClO4.
(4)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(5)某学习小组模拟工业流程图中的蒸馏过程,有液体流出时立即收集产品以获得HClO4纯品.请评价这一操作是否合理并说明理由不合理,因为水的沸点是100℃,HClO4的沸点是130℃,所以最先蒸馏流出的是水而不是HClO4.
查阅资料得到以下有关高氯酸的信息:
| 名称 | 分子式 | 外观 | 沸点 |
| 高氯酸 | HClO4 | 无色液体 | 130℃ |

(1)操作①的名称是过滤.
(2))Ca(ClO)2、ClO2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有强氧化性
(3)反应器Ⅰ中投料时需加入过量浓硫酸,请简述目的为了产物能得到HClO4而不是NaClO4.
(4)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(5)某学习小组模拟工业流程图中的蒸馏过程,有液体流出时立即收集产品以获得HClO4纯品.请评价这一操作是否合理并说明理由不合理,因为水的沸点是100℃,HClO4的沸点是130℃,所以最先蒸馏流出的是水而不是HClO4.
15.下列物质属于同分异构体的是( )
| A. | 麦芽糖和蔗糖 | B. | 蛋白质和氨基酸 | C. | 油和脂 | D. | 淀粉和纤维素 |
5.在标准状况下,如果2.8L氢气含有a个氢原子,则阿伏加德罗常数可表示为( )
| A. | amol-1 | B. | 2amol-1 | C. | 4amol-1 | D. | 8a mol-1 |
12.既能和盐酸反应,又能和烧碱溶液反应的盐是( )
| A. | 氧化铝 | B. | 氢氧化铝 | C. | 铝 | D. | 碳酸氢钠 |
10.下列化学用语正确的是( )
| A. | 聚丙烯的结构简式为: | B. | 丙烷分子的球棍模型为: | ||
| C. | 四氯化碳分子的电子式为: | D. | 苯的最简式为C6H6 |