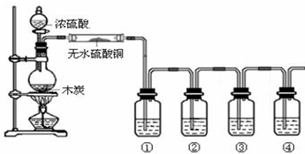
题目内容
10.依据下面的甲、乙、丙三图,判断下列叙述不正确的是( )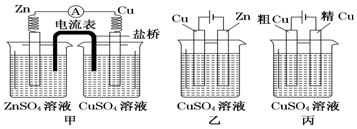
| A. | 甲是原电池,乙是电镀装置 | |
| B. | 甲、乙装置中,锌极上均发生氧化反应 | |
| C. | 乙装置中,铜极因发生氧化反应而溶解 | |
| D. | 乙装置中,c(Cu2+)不变,丙装置中,c(Cu2+)减小 |
分析 A.甲装置没有外加电源,属于原电池,乙装置存在外加电源,属于电解池;
B.在原电池的负极上发生氧化反应,在电解池的阴极上,发生还原反应;
C.在电解池的阳极上发生的是失电子的氧化反应;
D.电镀铜时溶液中铜离子浓度不变,精炼铜时溶液中铜离子浓度减小.
解答 解:A.甲装置没有外加电源,属于原电池,乙装置存在外加电源,属于电解池,可以在锌上镀铜,故A正确;
B.甲装置中,锌是负极,该电极上锌失电子发生氧化反应,乙装置中,锌极是阴极,该电极上发生还原反应,故B错误;
C.乙、丙装置中,阳极均是活泼的金属电极,该电极发生氧化反应而溶解,故C正确;
D.乙装置是电镀铜,阳极铜失电子生成铜离子进入溶液,阴极铜离子得电子析出铜,溶解的铜与析出的铜恰好相等,溶液中铜离子浓度不变;丙装置中,粗铜电极发生氧化反应,除铜失电子溶解外,还有活泼金属铁、锌、镍失电子,阴极只有铜离子得电子析出铜,阳极溶解的铜小于阴极析出的铜,溶液中铜离子浓度减小,故D正确;
故选B.
点评 本题考查学生原电池和电解池的工作原理知识,明确电镀池和电解精炼铜装置的特点是解题的关键,难度中等.

练习册系列答案
相关题目
20.化学反应中通常伴随着能量变化,下列说法中错误的是( )
| A. | 煤燃烧时并不能将化学能全部转化为热能 | |
| B. | 原电池将化学能转化为电能 | |
| C. | 二次电池放电时将电能转化为化学能 | |
| D. | 镁条燃烧时将部分化学能转化为光能 |
1.在恒容绝热的密闭容器中进行可逆反应;X(g)+2Y(g)?Z(s)+2W(g).已知开始时各物质的物质的量如表,反应达到平衡后,密闭容器体系内压强增大.下列判断正确的是( )
| 物质 | X | Y | Z | W |
| 物质的量/mol | 1.00 | 2.00 | 0 | 2.00 |
| A. | 该可逆反应为反应前后气体体积恒定的反应 | |
| B. | 该可逆反应的正反应为放热反应 | |
| C. | 达到平衡前,反应向逆反应方向进行 | |
| D. | 升高温度,平衡常数增大 |
18.足量的Zn与一定量的盐酸反应,由于反应速率太快,为减慢反应速率,但又不影响生成氢气的体积的是( )
| A. | NaOH固体 | B. | Na2CO3固体 | C. | NaCl晶体 | D. | CH3COONa固体 |
5.将6.4gSO2和8.0gSO3相比较,下列结论中错误的是( )
| A. | 它们所含氧原子数目之比为2:3 | B. | 它们的体积之比为1:1 | ||
| C. | 它们所含原子数目之比为3:4 | D. | 它们的分子数目之比为1:1 |
15.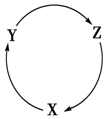 下列各组物质中,满足图中物质一步转化关系的选项是( )
下列各组物质中,满足图中物质一步转化关系的选项是( )
 下列各组物质中,满足图中物质一步转化关系的选项是( )
下列各组物质中,满足图中物质一步转化关系的选项是( )| X | Y | Z | |
| A | CO | CO2 | H2CO3 |
| B | Cu | CuO | Cu(OH)2 |
| C | CaO | Ca(OH)2 | CaCO3 |
| D | H2SO4 | Na2SO4 | NaCl |
| A. | A | B. | B | C. | C | D. | D |
 ;
;