题目内容
15.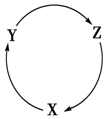 下列各组物质中,满足图中物质一步转化关系的选项是( )
下列各组物质中,满足图中物质一步转化关系的选项是( )| X | Y | Z | |
| A | CO | CO2 | H2CO3 |
| B | Cu | CuO | Cu(OH)2 |
| C | CaO | Ca(OH)2 | CaCO3 |
| D | H2SO4 | Na2SO4 | NaCl |
| A. | A | B. | B | C. | C | D. | D |
分析 A.H2CO3不能转化得到CO;
B.氧化铜不能与水反应;
C.氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应得到碳酸钙,碳酸钙分解得到氧化钙;
D.用氯化钠不能制得硫酸.
解答 解:A.CO与氧气反应得到CO2,CO2与水反应可以得到H2CO3,H2CO3不能转化得到CO,故A不符合;
B.铜燃烧得到氧化铜,氧化铜不能与水反应生成氢氧化铜,故B不符合;
C.氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应得到碳酸钙,碳酸钙分解得到氧化钙,故C符合;
D.硫酸与氢氧化反应得到硫酸钠,硫酸钠与氯化钡反应得氯化钠,用氯化钠不能制得硫酸,故D不符合.
故选C.
点评 本题考查考生对常见元素及其化合物知识的掌握情况,可用代入法,即把各选项中的X、Y、Z代入右图的圆圈中进行判断,题目难度不大.

练习册系列答案
相关题目
5.已知H-H 键的键能为436kJ•mol-1,Cl-Cl键的键能为243kJ•mol-1,H-Cl键的键能为431kJ•mol-1,则H2 (g )+Cl2(g )═2HCl(g ) 的反应热(△H )等于( )
| A. | -183 kJ•mol-1 | B. | +183 kJ•mol-1 | C. | -862 kJ•mol-1 | D. | +862 kJ•mol-1 |
6.下列说法中正确的是( )
| A. | 氢氧化钠的摩尔质量是40g | |
| B. | 1mol氢氧根离子的质量是17g | |
| C. | 1mol氮的质量是14g/mol | |
| D. | 氩气的摩尔质量就是它的相对原子质量 |
3.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,22.4 L水中含有的水分子数为NA | |
| B. | 常温常压下,46 g NO2和N2O4的混合气体中含有的氧原子数为2NA | |
| C. | 1mol/L的Ba(NO3)2溶液中含NO3-离子数为2NA | |
| D. | 分子数为NA的CO和N2的混合气体的体积约为22.4 L,质量为28 g |
10.依据下面的甲、乙、丙三图,判断下列叙述不正确的是( )
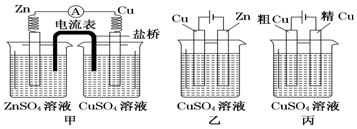

| A. | 甲是原电池,乙是电镀装置 | |
| B. | 甲、乙装置中,锌极上均发生氧化反应 | |
| C. | 乙装置中,铜极因发生氧化反应而溶解 | |
| D. | 乙装置中,c(Cu2+)不变,丙装置中,c(Cu2+)减小 |
20.下列各组微粒半径大小的比较,错误的是( )
| A. | K>Na>Li | B. | Na+>Mg2+>O2- | C. | P>S>O | D. | Cl-<Br-<I- |
4.下列叙述正确的是( )
| A. | 钠的摩尔质量等于它的相对原子质量 | |
| B. | CH4的摩尔质量为16 g/mol | |
| C. | 22.4 L任何气体的物质的量均为1 mol | |
| D. | 1 mol 任何物质均含有NA个分子 |
