题目内容
2.已知:W、Y、Z、T、M为前四周期元素,且原子半径依次增大.请填空:(1)W、Z是形成化合物种类最多的两种元素,写出Z原子的核外电子排布图
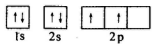 ;
;(2)化合物YW3极易溶于水的原因H2O与NH3形成氢键;YW3的分子构型为三角锥形.YW3属于极性(填“极性”或“非极性”)分子,其中Y的化合价为-3.
(3)元素T的原子中电子共占据了7个轨道,则T在元素周期表第三周期IIIA族.T的化合物TY熔融时不导电,常用作砂轮及耐高温材料,由此推知,它属于b(填编号字母);
a.离子晶体 b.原子晶体 c.分子晶体 d.无法判断
(4)M3+的3d轨道为半充满,则M的原子的电子排布式为1s22s22p63s23p63d64s2,M位于周期表的d区(按电子的填入顺序划分),M的晶体中的粒子采用的是体心立方堆积,则该种堆积方式的配位数为8,若其晶胞的边长为acm,M的摩尔质量为Mr g/mol,阿伏加德罗常数的值为NA,则其密度为$\frac{2M}{{a}^{3}{N}_{A}}$g/cm3.
分析 W、Y、Z、T、M为前四周期元素,且原子半径依次增大,W、Z是形成化合物种类最多的两种元素,为C、H元素,W原子半径小于Z,则W是H、Z是C元素;
化合物YW3极易溶于水,该物质为氨气,则Y为N元素;
元素T的原子中电子共占据了7个轨道,为Al元素;
M3+的3d轨道为半充满,则M原子核外电子数=2+8+8+5+3=26,为Fe元素;
(1)Z为C元素,其原子核外有6个电子,根据构造原理书写C原子核外电子排布图;
(2)含有氢键的物质极易溶于水;氨气分子中N原子价层电子对个数是4且含有1个孤电子对,根据价层电子对互斥理论判断氨气分子空间构型,正负电荷中心不重合的分子为极性分子;
(3)主族元素原子核外电子层数与其周期数相同,最外层电子数与其族序数相同;分子晶体熔沸点较高、硬度较大,熔融状态下不导电;
(4)Fe原子核外电子数是26,根据构造原理书写Fe原子核外电子排布式;Fe元素位于d区,M的晶体中的粒子采用的是体心立方堆积,即该晶胞中体心上含有1个原子、每个顶点上含有一个原子;该晶胞中Fe原子个数=1+8×$\frac{1}{8}$=2,密度=$\frac{\frac{M}{{N}_{A}}×2}{V}$.
解答 解:W、Y、Z、T、M为前四周期元素,且原子半径依次增大,W、Z是形成化合物种类最多的两种元素,为C、H元素,W原子半径小于Z,则W是H、Z是C元素;
化合物YW3极易溶于水,该物质为氨气,则Y为N元素;
元素T的原子中电子共占据了7个轨道,为Al元素;
M3+的3d轨道为半充满,则M原子核外电子数=2+8+8+5+3=26,为Fe元素;
(1)Z为C元素,其原子核外有6个电子,根据构造原理书写C原子核外电子排布图为 ,故答案为:
,故答案为: ;
;
(2)H2O与 NH3形成氢键导致氨气易溶于水;氨气分子中N原子价层电子对个数是4且含有1个孤电子对,根据价层电子对互斥理论判断氨气分子空间构型为三角锥形,正负电荷中心不重合的分子为极性分子,氨气分子结构不对称,正负电荷中心不重合,为极性分子,氨气中H元素为+1价,则N元素为-3价,
故答案为:H2O与 NH3形成氢键;三角锥形;极性;-3;
(3)主族元素原子核外电子层数与其周期数相同,最外层电子数与其族序数相同,Al原子核外有3个电子层、最外层电子数是3,所以位于第三周期第IIIA族;分子晶体熔沸点较高、硬度较大,熔融状态下不导电,AlN熔沸点较高、硬度较大,为原子晶体,
故答案为:第三;IIIA;b;
(4)Fe原子核外电子数是26,根据构造原理书写Fe原子核外电子排布式为1s22s22p63s23p63d64s2;Fe元素位于d区,M的晶体中的粒子采用的是体心立方堆积,即该晶胞中体心上含有1个原子、每个顶点上含有一个原子,所以Fe原子配位数是8;该晶胞中Fe原子个数=1+8×$\frac{1}{8}$=2,密度=$\frac{\frac{M}{{N}_{A}}×2}{V}$=$\frac{\frac{M}{{N}_{A}}×2}{{a}^{3}}$=$\frac{2M}{{a}^{3}{N}_{A}}$g/cm3,
故答案为:1s22s22p63s23p63d64s2;d;8;$\frac{2M}{{a}^{3}{N}_{A}}$g/cm3.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、微粒空间构型判断、原子核外电子排布、氢键等知识点,侧重考查学生空间想象、计算及综合知识运用能力,熟练掌握体心立方、面心立方中原子在晶胞中的位置,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 金属元素的原子只有还原性、金属离子只有氧化性 | |
| B. | 金属元素在化合物中一定显正价 | |
| C. | 金属元素在不同化合物中的化合价都相同 | |
| D. | 金属元素的单质在常温下都呈固态 |
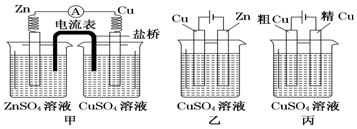
| A. | 甲是原电池,乙是电镀装置 | |
| B. | 甲、乙装置中,锌极上均发生氧化反应 | |
| C. | 乙装置中,铜极因发生氧化反应而溶解 | |
| D. | 乙装置中,c(Cu2+)不变,丙装置中,c(Cu2+)减小 |
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 没有明显变化 |
| ② | B+D | 有无色、无味气体生成 |
| ③ | B+C | 有白色沉淀生成 |
| ④ | A+D | 有白色沉淀生成 |
(1)A、B、C、D溶液中溶质的化学式:ACaCl2;BHCl;CAgNO3;DNa2CO3.
(2)写出实验顺序中发生反应的②③④中有关的离子方程式:②CO32-+2H+=CO2↑+H2O;③Cl-+Ag+=AgCl↓;④CO32-+Ca2+=CaCO3↓.