��Ŀ����
15���������ǽ������ϵ����ǣ���оƬ��ʹ�ã��ٽ�����Ϣ�����ĸ�������1���մɡ�ˮ��Ͳ��������ڴ�ͳ�����β��ϣ����У�������ͨ��������Ҫԭ�ϳ���SiO2��Na2CO3�CaCO3���������������з�����Na2CO3+SiO2$\frac{\underline{\;����\;}}{\;}$Na2SiO3+CO2�ķ�Ӧ��̼������ǿ�ڹ��ᣬ��Ϊʲô�÷�Ӧ���ڸ����·�����������Na2SiO3���ȶ��Ա�Na2CO3ǿ��
��2����ҵ���ᴿ���ж���·�ߣ�����һ�ֹ�������ʾ��ͼ����Ҫ��Ӧ��ͼ��
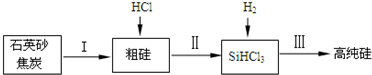
����д����Ӧ��Ļ�ѧ����ʽ����Si+3HCl$\frac{\underline{\;\;��\;\;}}{\;}$SiHCl3+H2����SiHCl3+H2$\frac{\underline{\;����\;}}{\;}$Si+3HCl��
������������Ӧ�IJ����У�SiHCl3��Լռ85%�������е��������ʵķе��������±���
| ���� | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| �е�/�� | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
A����¯���� B���ƾ��Ƽ��� C��ɰԡ���� D��ˮԡ����
��SiHCl3����ˮ�⣬����ȫˮ��ʱ�ķ�Ӧ����ʽΪSiHCl3+4H2O=H4SiO4+H2��+3HCl��
���� ��1��������ͨ��������Ҫԭ���У�SiO2��Na2CO3�Լ�CaCO3����Ӧ�����ɸ��ȶ����ʵķ�����У�
��2����ʯӢɰ�뽹̿��Ӧ�õ�Si��CO���ֹ���HCl��Ӧ�õ�SiHCl3���������������������ԭSiHCl3�õ��ߴ��ȹ裻
�ڳ�����ȥ�߷е�Ĺ裬�ڿ�������������Һ��ķе�Ӧ���ڿ����ķе㣬��Ҫ�е���Խϸߵ�SiCl4��SiHCl3�����߷е������ˮ�ķе㣬��������ˮԡ���ȣ�
��SiHCl3����ˮ�⣬����ȫˮ������ԭ���ᡢ������HCl��
��� �⣺��1��������ͨ��������Ҫԭ���У�SiO2��Na2CO3�Լ�CaCO3��̼������ǿ�ڹ��ᣬ�������¶���������̼���Ʒ�Ӧ���ɹ������������̼��˵��������Na2SiO3���ȶ��Ա�Na2CO3ǿ��
�ʴ�Ϊ��CaCO3��������Na2SiO3���ȶ��Ա�Na2CO3ǿ��
��2����ʯӢɰ�뽹̿��Ӧ�õ�Si��CO���ֹ���HCl��Ӧ�õ�SiHCl3���������������������ԭSiHCl3�õ��ߴ��ȹ裬��Ӧ��Ļ�ѧ����ʽΪ��Si+3HCl$\frac{\underline{\;\;��\;\;}}{\;}$SiHCl3+H2����Ӧ��Ļ�ѧ����ʽ����
�ʴ�Ϊ��Si+3HCl$\frac{\underline{\;\;��\;\;}}{\;}$SiHCl3+H2��SiHCl3+H2$\frac{\underline{\;����\;}}{\;}$Si+3HCl��
�ڳ�����ȥ�߷е�Ĺ裬�ڿ�������������Һ��ķе�Ӧ���ڿ����ķе㣬��Ҫ�е���Խϸߵ�SiCl4��SiHCl3�����߷е������ˮ�ķе㣬��������ˮԡ���ȣ����Ⱦ��ȣ�
�ʴ�Ϊ��Si��SiCl4��SiHCl3��D��
��SiHCl3����ˮ�⣬����ȫˮ������ԭ���ᡢ������HCl����Ӧ����ʽΪ��SiHCl3+4H2O=H4SiO4+H2��+3HCl��
�ʴ�Ϊ��SiHCl3+4H2O=H4SiO4+H2��+3HCl��
���� �����ǶԻ�ѧ�����Ŀ��飬�漰�����ι�ҵ������Ʊ����ᴿ��ע��Ի���֪ʶ���������գ�

 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�| A�� | MnO2��Ũ���ᷴӦ��Cl2��MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2Cl-+Cl2��+2H2O | |
| B�� | �Ȼ�����Һ�μӵ���ˮ�еõ�Fe��OH��3 ���壺Fe3++3H2O�TFe��OH��3��+3H+ | |
| C�� | �������������H2��2Fe+6H+�T2Fe3++3H2�� | |
| D�� | Ca��HCO3��2��Һ������NaOH��Һ��Ӧ��HCO3-+Ca2++OH-�TCaCO3��+H2O |
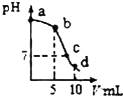 25��ʱ����10mL0.2mol•L-1NaCN��Һ�м���0.2mol•L-1���ᣬ��ҺpH��������������仯�������ͼ��ʾ����������˵������ȷ���ǣ���������֪��Ka��HCN��=6.4��10-10��
25��ʱ����10mL0.2mol•L-1NaCN��Һ�м���0.2mol•L-1���ᣬ��ҺpH��������������仯�������ͼ��ʾ����������˵������ȷ���ǣ���������֪��Ka��HCN��=6.4��10-10��| A�� | a��ʱ��CN-����Ũ�ȴ��������� | B�� | b��ʱ��c��HCN����c��CN-�� | ||
| C�� | c��ʱ��c��Na+��=c��Cl-��+c��CN-�� | D�� | d��ʱ����Һ��c��H+����8��10-5mol•L-1 |
��Na2O2��s��+CO2��g���TNa2CO3��s��+$\frac{1}{2}$O2��g����H=-226kJ•mol-1
���������Ȼ�ѧ����ʽ�жϣ�����˵����ȷ���ǣ�������
| A�� | Na2O2��s����CO2��g����Ӧʱ���ų�226kJ���� | |
| B�� | CO��ȼ����Ϊ��H=-566kJ/mol | |
| C�� | CO��g����Na2O2 ��S����Ӧ���Ȼ�ѧ����ʽΪ��Na2O2��s��+CO��g���TNa2CO3��s����H=-509kJ•mol-1 | |
| D�� | 2Na2O2��s��+2CO2��g���T2Na2CO3��s��+O2��g����H=-452kJ•mol-1 |
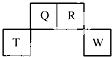 ������Ԫ��Q��R��T��W��Ԫ�����ڱ��е�λ����ͼ��ʾ������T��������������������������ȣ�
������Ԫ��Q��R��T��W��Ԫ�����ڱ��е�λ����ͼ��ʾ������T��������������������������ȣ�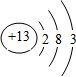 ��
�� ��Υ��������������ԭ����
��Υ��������������ԭ����
