题目内容
化合物G的合成路线如下:
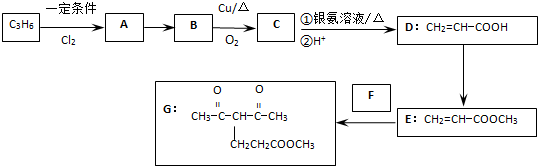
(1)D中含氧官能团的名称为 ,1mol G发生加成反应最多消耗 mol H2
(2)除掉E中含有少量D的试剂和操作是 ;下列有关E的说法正确的是 (填字母序号).
A.可发生氧化反应
B.催化条件下可发生缩聚反应
C.可发生取代反应
D.是CH2=CHCOOCH2CH3的同系物
E.易溶于水
(3)写出A→B的化学反应方程式 .
(4)反应E+F→G属于下列麦克尔加成反应类型,则F的结构简式为 .

(5)比G少2个氢原子的物质具有下列性质:①遇FeCl3溶液显紫色;②苯环上的一氯取代物只有一种;③1mol物质最多可消耗2mol Na和1mol NaOH.任写一种该物质的结构简式 .

(1)D中含氧官能团的名称为
(2)除掉E中含有少量D的试剂和操作是
A.可发生氧化反应
B.催化条件下可发生缩聚反应
C.可发生取代反应
D.是CH2=CHCOOCH2CH3的同系物
E.易溶于水
(3)写出A→B的化学反应方程式
(4)反应E+F→G属于下列麦克尔加成反应类型,则F的结构简式为

(5)比G少2个氢原子的物质具有下列性质:①遇FeCl3溶液显紫色;②苯环上的一氯取代物只有一种;③1mol物质最多可消耗2mol Na和1mol NaOH.任写一种该物质的结构简式
考点:有机物的合成
专题:有机物的化学性质及推断
分析:C3H6为CH2=CH-CH3,因为D为CH2=CH-COOH,所以CH2=CH-CH3与Cl2发生ɑ-H的取代反应,生成的A为CH2=CH-CH2Cl,A中Cl被羟基取代转化为B(CH2=CH-CH2OH),B催化氧化得到C(CH2=CH-CHO),C发生银镜反应生成D(CH2=CH-COOH),D与CH3OH发生酯化反应生成E,E与F发生加成反应生成G,据此分析解答.
解答:
解:C3H6为CH2=CH-CH3,因为D为CH2=CH-COOH,所以CH2=CH-CH3与Cl2发生ɑ-H的取代反应,生成的A为CH2=CH-CH2Cl,A中Cl被羟基取代转化为B(CH2=CH-CH2OH),B催化氧化得到C(CH2=CH-CHO),C发生银镜反应生成D(CH2=CH-COOH),D与CH3OH发生酯化反应生成E,E与F发生加成反应生成G,
(1)根据以上分析,D为CH2=CH-COOH,含氧官能团的名称为:羧基;根据G的结构简式,G中含有2个羰基,所以1mol G发生加成反应最多消耗2molH2,故答案为:羧基;2;
(2)根据以上分析,D为CH2=CH-COOH,E为CH2=CH-COOCH3,饱和碳酸钠溶液可与羧酸反应,所以除掉E中含有少量D的试剂为饱和碳酸钠溶液,反应后生成羧酸盐溶液,充分振荡后,静置,分液,或者蒸馏,或者先分液再蒸馏,即可提纯;
A、E中含有碳碳双键,可发生氧化反应,故正确;
B、E中含有的官能团为碳碳双键和酯基,不能发生缩聚反应,故错误;
C、E中含有酯基,可发生水解反应,属于取代反应,故正确;
D、E与CH2=CHCOOCH2CH3结构相似,分子组成相差一个CH2原子团,互为同系物,故正确;
E、E属于酯,难溶于水,故错误;
故答案为:向混合物中加入饱和碳酸钠溶液,充分振荡后,静置,分液,或者蒸馏,或者先分液再蒸馏;ACD;
(3)A→B 为CH2Cl-CH=CH2在氢氧化钠的水溶液中发生水解反应,生成氯代烃,化学方程式为CH2Cl-CH=CH2+H2O
CH2OH-CH=CH2+HCl,
故答案为:CH2Cl-CH=CH2+H2O
CH2OH-CH=CH2+HCl;
(4)根据以上分析,E中碳碳双键发生加成反应可得G,对比E、G的结构简式可得F为 ,故答案为:
,故答案为: ;
;
(5)比G少2个氢原子的物质的分子式为:C9H12O3,①遇FeCl3溶液显紫色,说明含有酚羟基;③1mol物质最多可消耗2molNa和1molNaOH,说明该物质含有1个醇羟基;再根据②苯环上的一氯取代物只有一种,可推出该物质的结构简式为: ,
,
故答案为: .
.
(1)根据以上分析,D为CH2=CH-COOH,含氧官能团的名称为:羧基;根据G的结构简式,G中含有2个羰基,所以1mol G发生加成反应最多消耗2molH2,故答案为:羧基;2;
(2)根据以上分析,D为CH2=CH-COOH,E为CH2=CH-COOCH3,饱和碳酸钠溶液可与羧酸反应,所以除掉E中含有少量D的试剂为饱和碳酸钠溶液,反应后生成羧酸盐溶液,充分振荡后,静置,分液,或者蒸馏,或者先分液再蒸馏,即可提纯;
A、E中含有碳碳双键,可发生氧化反应,故正确;
B、E中含有的官能团为碳碳双键和酯基,不能发生缩聚反应,故错误;
C、E中含有酯基,可发生水解反应,属于取代反应,故正确;
D、E与CH2=CHCOOCH2CH3结构相似,分子组成相差一个CH2原子团,互为同系物,故正确;
E、E属于酯,难溶于水,故错误;
故答案为:向混合物中加入饱和碳酸钠溶液,充分振荡后,静置,分液,或者蒸馏,或者先分液再蒸馏;ACD;
(3)A→B 为CH2Cl-CH=CH2在氢氧化钠的水溶液中发生水解反应,生成氯代烃,化学方程式为CH2Cl-CH=CH2+H2O
| NaOH |
| △ |
故答案为:CH2Cl-CH=CH2+H2O
| NaOH |
| △ |
(4)根据以上分析,E中碳碳双键发生加成反应可得G,对比E、G的结构简式可得F为
 ,故答案为:
,故答案为: ;
;(5)比G少2个氢原子的物质的分子式为:C9H12O3,①遇FeCl3溶液显紫色,说明含有酚羟基;③1mol物质最多可消耗2molNa和1molNaOH,说明该物质含有1个醇羟基;再根据②苯环上的一氯取代物只有一种,可推出该物质的结构简式为:
 ,
,故答案为:
 .
.
点评:本题考查有机物的合成,明确合成流程中各物质的推断是解答的关键,注意有机物的官能团与性质的关系即可解答,题目难度中等.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| B、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| C、三氯化铁溶液中加入铁粉:Fe3++Fe═2Fe2+ |
| D、向NaOH溶液中滴入少量AlCl3溶液:Al3++4OH-═AlO2-+2H2O |
下列实验可达到实验目的是:( )
①将CH3CH(OH)CH3与NaOH的醇溶液共热制备CH3CH=CH2
② 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备
③向CH3CH2Br中滴入AgNO3溶液以检验溴元素
④用溴水即可检验CH2=CH-CHO中的碳碳双键.
①将CH3CH(OH)CH3与NaOH的醇溶液共热制备CH3CH=CH2
②
 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备
③向CH3CH2Br中滴入AgNO3溶液以检验溴元素
④用溴水即可检验CH2=CH-CHO中的碳碳双键.
| A、只有① | B、只有①④ |
| C、只有①③④ | D、都不能 |
25℃时浓度都是1mol?L-1 的四种正盐溶液:AX、BX、AY、BY,AX的溶液pH=7且溶液中c(X-)=1mol?L-1 ,BX的溶液pH=4,BY溶液pH=6,下列说法正确的是( )
| A、电离平衡常数K(BOH)小于K(HY) |
| B、AY溶液的pH值小于BY的pH |
| C、稀释相同倍数,溶液pH值变化BX小于BY |
| D、将浓度均为1mol?L-1的HX和HY溶液分别稀释10倍后,HX溶液的pH大于HY |
我国国家药品监督管理局在2000年11月16日发出紧急通知,立即禁止使用含有PPA的抗感冒药物.PPA是盐酸苯丙醇胺的英文缩写,已知苯丙醇胺的结构简式如图所示,下列对苯丙醇胺叙述错误的是( )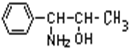
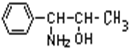
| A、一定条件下,可以发生消去反应 |
| B、一定条件下与Br2可以发生苯环上的取代反应 |
| C、具有弱碱性,可与强酸反应生成盐 |
| D、具有弱酸性,可与强碱反应生成盐 |
把NaHCO3和Na2CO3?10H2O混合物6.56g溶于水配成100mL溶液,c(Na+)=0.5mol/L.如将溶液蒸干、灼烧,所得固体为(2NaHCO3=Na2CO3+H2O+CO2↑条件:加热)( )
| A、2.65 g |
| B、2.96 g |
| C、6.56g |
| D、5.3g |
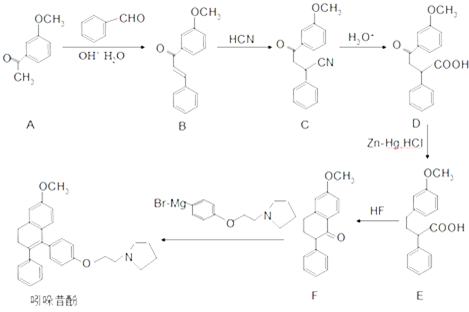
 ]是有机合成中间体,请设计合理的方案以丙酮
]是有机合成中间体,请设计合理的方案以丙酮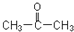 )为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,并注明反应条件).提示:①合成过程中无机试剂任选;
)为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,并注明反应条件).提示:①合成过程中无机试剂任选;
