题目内容
低碳烯烃在石油化工生产中有着广泛的应用,为解决石油资源日益紧缺的矛盾,当前正在研究开发生产低碳烯烃的新方法,其中由甲醇制乙烯、丙烯、丁烯的生产流程已经相对成熟,可以实现规模化生产.相关反应如下:
①2CH3OH(g)?C2H4(g)+2H2O(g)△H1=-24.19kJ?mol-1
②3CH3OH(g)?C3H6(g)+3H2O(g)△H2
③4CH3OH(g)?C4H8(g)+4H2O(g)△H3
④2CH3OH(g)?CH3OCH3(g)+H2O(g)△H4
请回答下列问题:
(1)判断反应①能否自发进行? (填“低于一定温度能自发进行”、“高于一定温度能自发进行”或“任何温度下都能自发进行”).
(2)已知,H2O(1)═H2O(g)△H=+44kJ?mol-1.表示H2和CH2=CH2标准燃烧的热化学方程式分别为:H2+
O2(g)═H2O(1)△H=-285.8kJ?mol-1.CH2=CH2+3O2(g)═2CO2(g)+2H2O(g)(1)△H=-1411kJ/mol
则表示CH3OH标准燃烧的热化学方程式为 .
(3)已知反应②、③的平衡常数如下,下列叙述正确的是 (填字母序号)
A、△H2>0,△H3<0
B、相同条件下,达到平衡时的甲醇的转化率:反应③>②
C、从平衡常数推测,相同条件下反应③的反应速率肯定比反应②的反应速率大.
①2CH3OH(g)?C2H4(g)+2H2O(g)△H1=-24.19kJ?mol-1
②3CH3OH(g)?C3H6(g)+3H2O(g)△H2
③4CH3OH(g)?C4H8(g)+4H2O(g)△H3
④2CH3OH(g)?CH3OCH3(g)+H2O(g)△H4
请回答下列问题:
(1)判断反应①能否自发进行?
(2)已知,H2O(1)═H2O(g)△H=+44kJ?mol-1.表示H2和CH2=CH2标准燃烧的热化学方程式分别为:H2+
| 1 |
| 2 |
则表示CH3OH标准燃烧的热化学方程式为
(3)已知反应②、③的平衡常数如下,下列叙述正确的是
| 温度(℃) | 300 | 400 | 500 |
| K② | 3.1×1015 | 1.66×1014 | 5.3×1013 |
| K③ | 4.0×1020 | 3.6×1018 | 5.7×1017 |
B、相同条件下,达到平衡时的甲醇的转化率:反应③>②
C、从平衡常数推测,相同条件下反应③的反应速率肯定比反应②的反应速率大.
考点:热化学方程式,焓变和熵变,用化学平衡常数进行计算
专题:
分析:(1)如反应能自发进行,应满足△H-T?△S<0;
(2)已知①2CH3OH(g)?C2H4(g)+2H2O(g)△H1=-24.19kJ?mol-1,②H2O(1)═H2O(g)△H=+44kJ?mol-1,③CH2=CH2+3O2(g)═2CO2(g)+2H2O(g)△H=-1411kJ/mol,利用盖斯定律将①+③-②×2可得CH3OH标准燃烧的热化学方程式;
(3)由表中数据可知,温度升高,平衡常数减小,则都为放热反应,平衡常数越大,转化率越大,但不能用于比较反应速率大小.
(2)已知①2CH3OH(g)?C2H4(g)+2H2O(g)△H1=-24.19kJ?mol-1,②H2O(1)═H2O(g)△H=+44kJ?mol-1,③CH2=CH2+3O2(g)═2CO2(g)+2H2O(g)△H=-1411kJ/mol,利用盖斯定律将①+③-②×2可得CH3OH标准燃烧的热化学方程式;
(3)由表中数据可知,温度升高,平衡常数减小,则都为放热反应,平衡常数越大,转化率越大,但不能用于比较反应速率大小.
解答:
解:(1)因△S>0,如反应能自发进行,应满足△H-T?△S<0,一般情况下能进行,但温度不能过低,应在较高温度下进行反应,
故答案为:高于一定温度能自发进行;
(2)已知①2CH3OH(g)?C2H4(g)+2H2O(g)△H1=-24.19kJ?mol-1,②H2O(1)═H2O(g)△H=+44kJ?mol-1,③CH2=CH2+3O2(g)═2CO2(g)+2H2O(g)△H=-1411kJ/mol,利用盖斯定律将①+③-②×2可得2CH3OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H=(-24.19kJ?mol-1)+(-1411kJ/mol)-2×(+44kJ?mol-1)=-1523.9kJ/mol,故答案为:2CH3OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H=-1523.9kJ/mol;
(3)由表中数据可知,温度升高,平衡常数减小,则都为放热反应,平衡常数越大,转化率越大,但不能用于比较反应速率大小,只有B正确,故答案为:B.
故答案为:高于一定温度能自发进行;
(2)已知①2CH3OH(g)?C2H4(g)+2H2O(g)△H1=-24.19kJ?mol-1,②H2O(1)═H2O(g)△H=+44kJ?mol-1,③CH2=CH2+3O2(g)═2CO2(g)+2H2O(g)△H=-1411kJ/mol,利用盖斯定律将①+③-②×2可得2CH3OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H=(-24.19kJ?mol-1)+(-1411kJ/mol)-2×(+44kJ?mol-1)=-1523.9kJ/mol,故答案为:2CH3OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H=-1523.9kJ/mol;
(3)由表中数据可知,温度升高,平衡常数减小,则都为放热反应,平衡常数越大,转化率越大,但不能用于比较反应速率大小,只有B正确,故答案为:B.
点评:本题综合考查化学反应与能量,化学平衡等知识,为高频考点,侧重学生的分析能量和计算能量的考查,注意把握盖斯定律的应用以及平衡常数的意义,难度中等.

练习册系列答案
相关题目
有28gCuO和MgO固体混合物与200ml硫酸恰好完全反应,将反应后的溶液小心蒸干,得到固体68g.则原硫酸溶液的物质的量浓度和原固体混合物中氧元素的质量分数分别是( )
| A、2.5mol?L-1 28.57% |
| B、2.2mol?L-1 23.07% |
| C、1.5mol?L-1 24.55% |
| D、2.5mol?L-1 18.37% |
实验是化学研究的基础,下列各图所示的实验方法、装置或操作正确的是( )
A、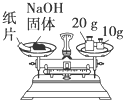 称量NaOH固体 |
B、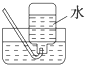 收集氯气 |
C、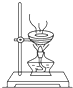 加热蒸发Nacl溶液 |
D、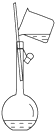 向容量瓶中转移溶液 |
 已知:X、Y、Z、W是四种短周期元素,它们的原子序数依次增大.其中X、Y、Z同周期,X与W同主族;X与Z形成的常见化合物之一常被用于高炉炼铁,且X、Z原子的L层都有2个未成对电子;Q+离子M层3d轨道电子为全充满状态.请回答下列问题:
已知:X、Y、Z、W是四种短周期元素,它们的原子序数依次增大.其中X、Y、Z同周期,X与W同主族;X与Z形成的常见化合物之一常被用于高炉炼铁,且X、Z原子的L层都有2个未成对电子;Q+离子M层3d轨道电子为全充满状态.请回答下列问题:
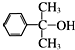 也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是
也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是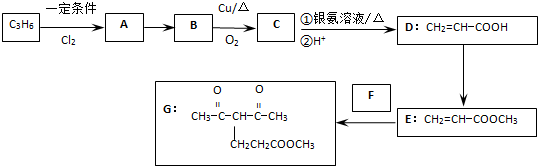

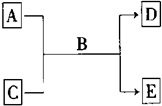 A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:
A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系: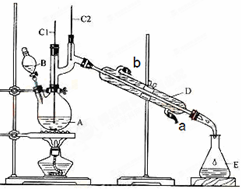 正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如下:
正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如下: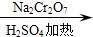 CH3CH2CH2CHO
CH3CH2CH2CHO