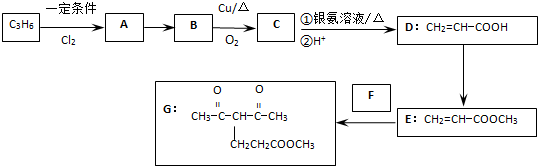
题目内容
把NaHCO3和Na2CO3?10H2O混合物6.56g溶于水配成100mL溶液,c(Na+)=0.5mol/L.如将溶液蒸干、灼烧,所得固体为(2NaHCO3=Na2CO3+H2O+CO2↑条件:加热)( )
| A、2.65 g |
| B、2.96 g |
| C、6.56g |
| D、5.3g |
考点:有关混合物反应的计算
专题:
分析:固体混合物加热至恒重时,剩余固体为Na2CO3,根据Na元素守恒计算出剩余固体Na2CO3的物质的量,再根据m=nM计算Na2CO3质量.
解答:
解:100mL溶液中c(Na+)=0.2mol?L-1,则n(Na+)=0.1L×0.5mol?L-1=0.05mol,
固体混合物加热至恒重时,剩余固体为Na2CO3,由钠元素守恒,则n(Na2CO3)=
=0.025mol,
m(Na2CO3)=0.025mol×106g/mol=2.65g,
故选A.
固体混合物加热至恒重时,剩余固体为Na2CO3,由钠元素守恒,则n(Na2CO3)=
| 0.05mol |
| 2 |
m(Na2CO3)=0.025mol×106g/mol=2.65g,
故选A.
点评:本题考查混合物的计算,为高频考点,注意加热后剩余固体的成分为碳酸钠,结合钠元素质量守恒计算为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列实验基本操作(或实验注意事项)中,主要是出于实验安全考虑的是( )
| A、气体实验装置在实验前进行气密性检查 |
| B、可燃性气体点燃前需要验纯 |
| C、实验剩余的药品不能放回原试剂瓶 |
| D、滴管不能交叉使用 |
容积完全相同的两个容器甲和乙,已知甲中装有SO2、O2各1mol,乙中装有SO2、O2各2mol,在同一温度下反应,2SO2(g)+O2(g)?2SO3(g)达平衡时,下列比较不正确的是( )
| A、反应速率:甲<乙 |
| B、O2浓度:甲<乙 |
| C、O2的转化率:甲<乙 |
| D、SO2的百分含量:甲<乙 |
实验是化学研究的基础,下列各图所示的实验方法、装置或操作正确的是( )
A、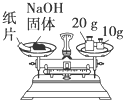 称量NaOH固体 |
B、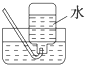 收集氯气 |
C、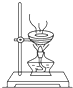 加热蒸发Nacl溶液 |
D、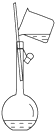 向容量瓶中转移溶液 |
下列说法正确的是( )
| A、仅用AgNO3溶液便可鉴别亚硝酸钠和食盐 |
| B、重结晶时,溶液冷却速度越慢得到的晶体颗粒越大 |
| C、乙酸与乙醇的混合液可用分液漏斗进行分离 |
| D、可用10mL5mol.L-1的高锰酸钾溶液检验火柴燃烧后生成的气体中是否含有SO2 |
下列两种无色试剂,不用其它试剂无法鉴别的是( )
| A、NaHCO3、HCl |
| B、Na2CO3、HCl |
| C、NaAlO2、H2SO4 |
| D、AlCl3、NaOH |
下列气体中,不能用排空气法收集的是( )
| A、Cl2 |
| B、CO2 |
| C、CO |
| D、O2 |
某温度下,满足下列条件的溶液肯定呈酸性的是( )
| A、加酚酞显无色的溶液 |
| B、含有H+的溶液 |
| C、pH<7的溶液 |
| D、CH3COOH和NH3?H2O混合液,当c(CH3COO-)>c(NH4+)时 |