题目内容
5.检验乙醇中是否含有水的方法为向乙醇中加入无水CuSO4粉末,若有蓝色物质生成,说明乙醇中含有水分,若无蓝色物质生成,说明乙醇中没有水分.分析 无水硫酸铜遇水变蓝,而乙醇不能,以此可检验水.
解答 解:检验乙醇中是否含有水的方法为向乙醇中加入无水CuSO4粉末,若有蓝色物质生成,说明乙醇中含有水分,若无蓝色物质生成,说明乙醇中没有水分,
故答案为:向乙醇中加入无水CuSO4粉末,若有蓝色物质生成,说明乙醇中含有水分,若无蓝色物质生成,说明乙醇中没有水分.
点评 本题考查物质的鉴别和检验,为高频考点,把握无水硫酸铜遇水变蓝的性质为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.如图是元素周期表主族元素的一部分
短周期元素X的最高正价是+5价,Y单质可在空气中燃烧.
(1)X元素在周期表中的位置:第三周期ⅤA族.
(2)Z的原子结构示意图: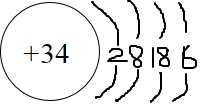 .
.
(3)W的最高价氧化物能溶于烧碱溶液,反应的化学方程式为:SiO2+2NaOH=Na2SiO3+H2O.
(4)探寻同一主族元素性质的一些共同规律,是学习化学的重要方法之一.在下表中列出对H2ZO3各种不同化学性质的推测,举例并写出相应的化学方程式.
| W | X | Y |
| Z |
(1)X元素在周期表中的位置:第三周期ⅤA族.
(2)Z的原子结构示意图:
 .
.(3)W的最高价氧化物能溶于烧碱溶液,反应的化学方程式为:SiO2+2NaOH=Na2SiO3+H2O.
(4)探寻同一主族元素性质的一些共同规律,是学习化学的重要方法之一.在下表中列出对H2ZO3各种不同化学性质的推测,举例并写出相应的化学方程式.
| 编号 | 性质推测 | 化学方程式 |
| 示例 | 氧化性 | H2ZO3+4HI═Z↓+2I2+1H2O |
| ① | 酸性 | H2SeO3+2NaOH=Na2SeO3+2H2O |
| ② | 还原性 | H2SeO3+Cl2+H2O=H2SeO4+2HCl |
16.下列说法正确的是( )
| A. | 用3mL稀硫酸溶液与足量Zn反应,当气泡稀少时加入5mL浓硫酸,又迅速产生较多气泡,由上述操作及现象得出结论:硫酸浓度增大,产生H2的反应速率加快 | |
| B. | FeCl3+3KSCN?Fe(SCN)3(血红色)+3KCl,向溶液中加入KCl固体可快速看到血红色 | |
| C. | Ba(OH)2•8H2O与NH4Cl的反应是放热反应 | |
| D. | 化学反应中的能量变化,通常表现为热量的变化 |
13.下列有关物质分类或归类中,正确的是( )
①混合物:盐酸、漂白粉、氯水、水玻璃 ②化合物:CaCl2、NaOH、HCl、HD
③电解质:明矾、生石膏、冰醋酸、氨水 ④酸性氧化物:SiO2 Mn2O7 N2O5 Cl2O7 .
①混合物:盐酸、漂白粉、氯水、水玻璃 ②化合物:CaCl2、NaOH、HCl、HD
③电解质:明矾、生石膏、冰醋酸、氨水 ④酸性氧化物:SiO2 Mn2O7 N2O5 Cl2O7 .
| A. | ①④ | B. | ②③ | C. | ③④ | D. | ③ |
20.化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况.下列反应中属于这种情况的是( )
①过量的锌与18mol/L的硫酸反应
②浓盐酸与过量的MnO2
③过量铜与浓硫酸
④过量稀硝酸与银反应
⑤过量稀硫酸与块状石灰石.
①过量的锌与18mol/L的硫酸反应
②浓盐酸与过量的MnO2
③过量铜与浓硫酸
④过量稀硝酸与银反应
⑤过量稀硫酸与块状石灰石.
| A. | ②③⑤ | B. | ②④ | C. | ①③④ | D. | ①②③④⑤ |
17.下列离子反应方程式正确的是( )
| A. | 向Na2SiO3溶液中逐滴加入少量稀盐酸:SiO32-+2H+═H2SiO3(胶体) | |
| B. | 将Cu片加入稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| C. | 向Na2S2O3溶液中加入稀硫酸:2S2O32-+2H+═SO42-+3S↓+H2O | |
| D. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-反应完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
14.下列物质溶于水时会破坏水的电离平衡,且属于电解质的是( )
| A. | 氯气 | B. | 氨气 | C. | 碘化钾 | D. | 碳酸氢钠 |
15.Na2CO3、NaHCO3、CaO和NaOH组成的混合物27.2g,溶于足量水并充分反应后,溶液中Ca2+、CO32-、HCO3-全部转化为沉淀,将反应容器内水分蒸干,最后得到白色固体29.0g.则原混合物中Na2CO3的质量是( )
| A. | 10.6 g | B. | 5.3 g | C. | 15.9 g | D. | 5.6 g |