题目内容
5.某探究小组为探究氯气的性质,并用装置F制取少量“漂白液”,设计了如下实验装置.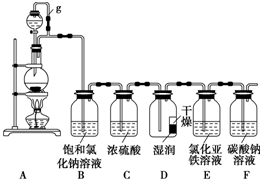
请回答下列问题:
(1)写出实验室制氯气的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)装置A中g管作用是平衡压强,使液体能顺利地滴入烧瓶中,
装置B的作用是除去氯气中混有的氯化氢,
装置C的作用是干燥氯气.
(3)反应一段时间后用注射器从E中抽取少量溶液,检验有Fe3+生成,请写出检验方法将抽取出的溶液注入试管中,向试管中滴加少量KSCN溶液,若溶液变红,则证明有Fe3+生成.
(4)已知HCO3-的酸性弱于次氯酸,请写出少量的氯气与F中足量的碳酸钠溶液反应的化学方程式:Cl2+2Na2CO3+H2O═NaCl+NaClO+2NaHCO3.
分析 (1)实验室利用浓盐酸与二氧化锰在加热条件下制备氯气,反应生成氯化锰、氯气与水;
(2)A为氯气发生装置,装置内压强增大,g可以平衡压强,使液体能顺利地滴入烧瓶中,由于盐酸易挥发,制备的氯气中含有HCl,饱和食盐水吸收HCl,用浓硫酸干燥氯气,D装置说明氯气无漂白性,是氯气和水反应生成的次氯酸具有漂白性,通过装置E中的氯化亚铁溶液,发生反应2Fe2++Cl2=2Fe3++2Cl-,可以验证氯气具有氧化性,最后通过碳酸钠溶液,而HClO酸性比弱,故少量氯气反应得到NaCl、碳酸氢钠与水;
(3)利用KSCN溶液检验铁离子,溶液变红,说明生成铁离子;
(4)HClO的酸性比碳酸弱,比碳酸氢根强,故少量氯气与碳酸钠溶液反应生成氯化钠、次氯酸钠与碳酸氢钠.
解答 解:(1)实验室利用浓盐酸与二氧化锰在加热条件下制备氯气,反应生成氯化锰、氯气与水,反应离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)A为氯气发生装置,装置内压强增大,g可以平衡压强,使液体能顺利地滴入烧瓶中,由于盐酸易挥发,制备的氯气中含有HCl,饱和食盐水吸收HCl,用浓硫酸干燥氯气,D装置说明氯气无漂白性,是氯气和水反应生成的次氯酸具有漂白性,通过装置E中的氯化亚铁溶液,发生反应2Fe2++Cl2=2Fe3++2Cl-,可以验证氯气具有氧化性,最后通过碳酸钠溶液,而HClO酸性比弱,故少量氯气反应得到NaCl、碳酸氢钠与水,则:
装置A中g管作用是:平衡压强,使液体能顺利地滴入烧瓶中,
装置B的作用是:除去氯气中混有的氯化氢,
装置C的作用是:干燥氯气,
故答案为:平衡压强,使液体能顺利地滴入烧瓶中;除去氯气中混有的氯化氢;干燥氯气;
(3)检验E的溶液中有Fe3+生成的方法:将抽取出的溶液注入试管中,向试管中滴加少量KSCN溶液,若溶液变红,则证明有Fe3+生成,
故答案为:将抽取出的溶液注入试管中,向试管中滴加少量KSCN溶液,若溶液变红,则证明有Fe3+生成;
(4)HClO的酸性比碳酸弱,比碳酸氢根强,故少量氯气与碳酸钠溶液反应生成氯化钠、次氯酸钠与碳酸氢钠,反应方程式为:Cl2+2Na2CO3+H2O═NaCl+NaClO+2NaHCO3,
故答案为:Cl2+2Na2CO3+H2O═NaCl+NaClO+2NaHCO3.
点评 本题以少量漂白液制取为载体,考查氯气实验制备与氯气的性质实验,涉及对装置的分析与评价、铁离子检验、信息获取与迁移应用等,关键是明确实验原理与各装置的作用,难度中等.

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案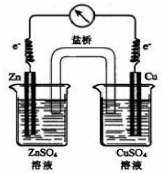
| A. | 该装置可以将化学能转变为电能 | B. | 电子由锌电极向铜电极移动 | ||
| C. | 盐桥中的阴离子向锌电极移动 | D. | 锌电极为正极,发生氧化反应 |
| A. | 等体积等物质的量浓度的Na2CO3和Na2SO4溶液,Na2SO4溶液中的离子总数多于Na2CO3溶液 | |
| B. | 相同温度下,pH相等的NaHCO3溶液、NaClO溶液、NaOH溶液:c(NaClO)>c(NaHCO3)>c(NaOH) | |
| C. | 常温下,CH3COONa与HCl溶液混合所得中性溶液:c(Na+)=c(Cl-)>c(H+)=c(OH一) | |
| D. | 0.1 mol•L-1Na2CO3溶液与0.1mol•L-1NaHCO3溶液等体积混合所得溶液:c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
| A. | 在溴乙烷中直接加入AgNO3溶液 | |
| B. | 加蒸馏水,充分搅拌后,加入AgNO3溶液 | |
| C. | 加入NaOH的乙醇溶液,加热后加入AgNO3溶液 | |
| D. | 加入NaOH溶液加热,冷却后加入稀硝酸酸化,然后加入AgNO3溶液 |
| A. | 地下钢管连接锌板 | B. | 汽水底盘喷涂高分子膜 | ||
| C. | 铁件镀铜 | D. | 金属护拦表面涂漆 |
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下生成甲醇蒸气和水蒸气.图表示恒压容器中0.5molCO2和1.5molH2转化率达80%时的能量变化示意图.
①能判断该反应向正反应方向进行的是:B
A.v正(H2)=3v逆(CH3OH)

B.容器中混合气体的密度变大
C.容器中压强不变
D.2个C=O断裂的同时有6个H-H形成
②上述反应其他条件保持不变,在恒容条件下进行,平衡时H2的转化率将变小(填“变大”“变小”或“不变”)
③写出上述反应的热化学方程式:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49kJ•mol-1
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)═CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度℃ | 起始量mol | 平衡量mol | 达平衡所需时间min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值:$\frac{1}{6}$(填具体值或取值范围)
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为2mol,则此时v正<v逆(填“<”“>”或“=”)
(3)甲醇在一定条件下能转化为甲醛,碘量滴定法是测定甲醛的化学方法之一,其原理是在碱性介质(NaOH)中,碘转化为次碘酸钠和碘化钠,后将溶液中游离的甲醛氧化为甲酸钠,经适当酸化后,剩余的次碘酸钠和碘化钠又生成碘,上述过程中甲醛参与的化学反应的离子方程式为:HCHO+IO-+OH-=HCOO-+I-+H2O.
| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度/(g/100g水) |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
(2)醇可发生分子内脱水生成烯烃,如C2H5OH$?_{170℃}^{浓硫酸}$CH2═CH2↑+H2O
请回答有关问题
Ⅰ.乙酸正丁酯粗产品的制备
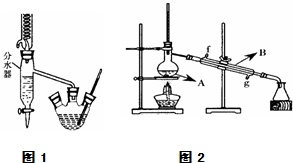
在三孔圆底烧瓶中装入沸石,加入18.5mL正丁醇和15.4mL冰醋酸(稍过量),再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)三孔烧瓶和蒸馏烧瓶在加热时都需要加入沸石,加入沸石是作用是防暴沸.本实验过程中可能产生多种有机副产品,请写成其中一种的结构简式CH3CH2CH2CH2OCH2CH2CH2CH3或CH2=CHCH2CH3.
(2)反应时加热有利于提高酯的产率,但实验发现温度过高酯的产率反而降低,可能的原因是乙酸、正丁醇都易挥发,温度过高可能使乙酸、正丁醇大量挥发使产率降低,温度过高可能发生副反应使产率降低.
Ⅱ.乙酸正丁酯粗产品的精制.
(3)将三孔圆底烧瓶中的产物转入分液漏斗中,并用饱和Na2CO3溶液洗涤有机层,接下来进行的操作名称是分液.
(4)将酯层采用如图2所示装置蒸馏.
①图2中仪器B的名称为冷凝管,水的流向应该从g(“f”或“g”)口进入.
②蒸馏收集乙酸正丁酯粗产品时,应将温度控制在126.1℃左右.