题目内容
18.下列说法正确的是( )| A. | 1molOH-的质量是17g | B. | 1mol气体所占的体积等于22.4L | ||
| C. | 氢气的摩尔质量是2g | D. | 摩尔是物质的质量单位 |
分析 A.结合m=nM计算;
B.状况未知,Vm不确定,V=nVm;
C.摩尔质量的单位为g/mol;
D.物质的量的单位为摩尔.
解答 解:A.1molOH-的质量是1mol×17g/mol=17g,故A正确;
B.Vm未知,不能计算1mol气体的体积,故B错误;
C.氢气的摩尔质量是2g/mol,故C错误;
D.摩尔是物质的量的单位,不是质量的单位,故D错误;
故选A.
点评 本题考查物质的量的计算,为高频考点,把握物质的量与质量、摩尔质量为解答的关键,侧重分析与计算能力的考查,注意选项B为易错点,题目难度不大.

练习册系列答案
相关题目
2.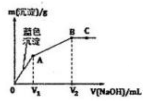 向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
 向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )| A. | 水的电离程度:A>B>C | |
| B. | 该实验不能证明Cu(OH)2的Ksp比Mg(OH)2的Ksp小 | |
| C. | 原溶液中MgCl2和CuCl2的物质的量浓度相等 | |
| D. | 若向Mg(OH)2悬浊液中加入CuCl2溶液,一定会有Cu(OH)2生成 |
6.下列有关推断中,不正确的是( )
| 事 实 | 结 论 | |
| A | CaCO3+2CH3COOH=(CH3COO)2Ca+CO2↑+H2O | 酸性:CH3COOH>H2CO3 |
| B | 氢硫酸(H2S)放置在空气中变浑浊 | 氧化性:O2>S |
| C | Al(OH)3既溶于强酸又溶于强碱 | Al元素既有金属性也有非金属性 |
| D | 反应A+2B?C达平衡后,升高温度平衡正向移动 | 升高温度,使v正增大、v逆减小 |
| A. | A | B. | B | C. | C | D. | D |
13.对于反应N2+O2$\frac{\underline{\;一定条件\;}}{\;}$2NO在密闭容器中进行,下列哪些条件能加快反应的速率( )
| A. | 缩小体积使压强增大 | B. | 增大体积使压强减小 | ||
| C. | 体积不变充入H2使压强增大 | D. | 压强不变充入N2使体积增大 |
3.可确认发生了化学平衡移动的是( )
| A. | 化学反应速率发生了改变 | |
| B. | 有气态物质参加的可逆反应达到平衡后,改变了压强 | |
| C. | 某一条件的改变,使正、逆反应速率不再相等 | |
| D. | 可逆反应达到平衡,使用了催化剂 |
10.下列离子方程式书写正确的是( )
| A. | 向饱和碳酸氢钙溶液中加入过量的NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| B. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═NH3•H2O+Al(OH)3↓+2BaSO4↓ | |
| C. | 氢氧化钠溶液吸收足量SO2气体:SO2+2OH-═SO32-+H2O | |
| D. | 标准状况下,将1.12LCO2气体通入1L0.1mol/L的NaAlO2溶液中:CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- |
7.下列关于热化学反应的描述中正确的是( )
| A. | HCl和NaOH反应的中和热△H=-57.3 kJ•mol-1,则H2SO4和Ba(OH)2反应热△H=2×(-57.3)kJ•mol-1 | |
| B. | 1 mol甲烷燃烧生成气态水和二氧化碳气体所放出的热量就是甲烷的燃烧热 | |
| C. | CO(g)的燃烧热是283.0 kJ•mol-1,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0 kJ•mol-1 | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
8.下列说法正确的是( )
| A. | 铁与盐酸反应生成氯化铁和氢气 | |
| B. | 铁在高温下与水蒸气的反应是置换反应 | |
| C. | 铁与盐酸、水蒸气反应,均作还原剂 | |
| D. | 铁丝在空气、纯氧中均不能燃烧 |
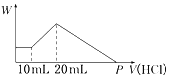 医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含量.回答下列问题:
医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含量.回答下列问题: