题目内容
13.对于反应N2+O2$\frac{\underline{\;一定条件\;}}{\;}$2NO在密闭容器中进行,下列哪些条件能加快反应的速率( )| A. | 缩小体积使压强增大 | B. | 增大体积使压强减小 | ||
| C. | 体积不变充入H2使压强增大 | D. | 压强不变充入N2使体积增大 |
分析 影响化学反应速率的条件有温度、浓度、压强以及催化剂等因素,注意压强增大时浓度必须增大,否则反应速率不会增大,以此解答该题.
解答 解:A.缩小体积,反应物的浓度增大,反应速率增大,故A正确;
B.增大体积,反应物的浓度减小,单位体积活化分子的数目减少,反应速率减慢,故B错误;
C.体积不变充入H2使压强增大(不考虑氢气与氧气的反应),但参加反应的物质的浓度不变,反应速率不变,故C错误;
D.压强不变充入N2使体积增大,氮气的浓度增大,但氧气、NO的浓度减小,反应速率不一定增大,可能减小,故D错误.
故选A.
点评 本题考查影响化学反应速率的外界因素的适用范围,为高频考点,明确温度、压强、浓度、催化剂等常见的对反应的影响因素是解答的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.一定质量的甲烷燃烧后的产物为CO、CO2和水蒸气,此混合气体质量为99.2g,当其缓慢经过无水CaCl2时,CaCl2增重50.4g.原混合气体中CO2的质量为( )
| A. | 13.2 g | B. | 22.4g | C. | 24.4g | D. | 26.4g |
1.有时候,将氧化还原反应方程式拆开写成两个“半反应”.下面是一个“半反应”式:MnO4-+____H++____e---____Mn2++____H2O
该反应方程式的配平化学计量数是( )
该反应方程式的配平化学计量数是( )
| A. | 1,8,4,1,4 | B. | 2,16,5,2,8 | C. | 1,6,5,1,3 | D. | 1,8,5,1,4 |
18.下列说法正确的是( )
| A. | 1molOH-的质量是17g | B. | 1mol气体所占的体积等于22.4L | ||
| C. | 氢气的摩尔质量是2g | D. | 摩尔是物质的质量单位 |
5.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol氦气中有2NA个氦原子 | |
| B. | 14 g氮气中含6.02×1023个氮原子 | |
| C. | 2 L 0.3 mol•L-1 Na2SO4溶液中含0.6 NA个Na+ | |
| D. | 18 g水中所含的电子数为10NA |
3.下列说法正确的是( )
| A. | 可用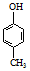 和HCHO 为原料合成 和HCHO 为原料合成 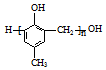 | |
| B. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| C. | C3H8的六氯代物共有4种,而且CH3-CH=CH-CH3与C3H6一定互为同系物 | |
| D. | 将0.1 mol/L的NaOH溶液与0.5 mol/L的CuSO4溶液等体积混合制得氢氧化铜悬浊液,用于检验麦芽糖是还原糖 |
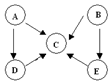 A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D在常温下都是气体,B为红棕色.
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D在常温下都是气体,B为红棕色.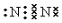 ,D的结构式:
,D的结构式: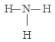 .
.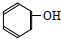 ②
② ③
③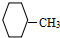 ④
④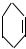 ⑤
⑤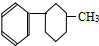 ⑥
⑥
 ⑧
⑧ ⑨
⑨ ⑩
⑩



